
���� ��1������������ת������������ͭ������þ��
��2��KspС����ת��Ϊ������������Һ��c��Mg2+����c��Cu2+��=$\frac{Ksp[Mg��OH��_{2}]}{Ksp[Cu��OH��_{2}]}$��
��3��ʹCu2+Ũ�Ƚ���ԭ����ǧ��֮һ��c��Cu2+��=$\frac{0.2mol/L}{1000}$=2��10-4mol/L�����Ksp[Cu��OH��2]=2��10-20���㣮
��� �⣺��1����Mg��OH��2��Һ����μ���CuSO4��Һ������������ת������Ӧ�����ӷ���ʽΪMg��OH��2+Cu2+=Mg2++Cu��OH��2��
�ʴ�Ϊ��Mg��OH��2+Cu2+=Mg2++Cu��OH��2��
��2����Ks��֪��������ͭ�����ܣ�����Mg2+��Cu2+��Ϊ0.1mol/l����Һ����μ������NaOH��Һ���ȳ���������ΪCu2+��������Һ��c��Mg2+����c��Cu2+��=$\frac{2��1{0}^{-11}}{2��1{0}^{-20}}$=1��109��
�ʴ�Ϊ��Cu2+��1��109��
��3��ʹCu2+Ũ�Ƚ���ԭ����ǧ��֮һ��c��Cu2+��=$\frac{0.2mol/L}{1000}$=2��10-4mol/L��c��OH-��=$\sqrt{\frac{2��1{0}^{-20}}{2��1{0}^{-4}}}$=10-8mol/L����c��H+��=10-6mol/L����pH=6���ʴ�Ϊ��6��
���� ���⿼�����ܵ���ʵ��ܽ�ƽ�⼰���㣬Ϊ��Ƶ���㣬���ճ���ת�����ܶȻ��ļ���Ϊ���Ĺؼ������ط�������������Ŀ��飬ע��pH�ĵ��ڼ����㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
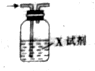 ��֪CO2ͨ�����ʯ��ˮ�У���Һ�ȱ���ǣ����ֱ���壮����ͼװ�ó�ȥCO2�����е�HCl��X�Լ�����ʵ��ǣ�������
��֪CO2ͨ�����ʯ��ˮ�У���Һ�ȱ���ǣ����ֱ���壮����ͼװ�ó�ȥCO2�����е�HCl��X�Լ�����ʵ��ǣ�������| A�� | NaOH��Һ | B�� | Ũ���� | C�� | Na2CO3��Һ | D�� | NaHCO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
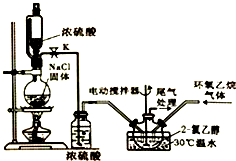 2-���Ҵ���һ����Ҫ���л�����ԭ�ϣ�����ʱ�ֽ⣮ͨ������������2-���Ҵ�Ϊ�ܼ������Ȼ����뻷�����鷴Ӧ�Ƶ��µ�2-���Ҵ�����ȡ��Ӧװ����ͼ��ʾ��
2-���Ҵ���һ����Ҫ���л�����ԭ�ϣ�����ʱ�ֽ⣮ͨ������������2-���Ҵ�Ϊ�ܼ������Ȼ����뻷�����鷴Ӧ�Ƶ��µ�2-���Ҵ�����ȡ��Ӧװ����ͼ��ʾ��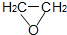 ��g��+HCl��g��?ClCH2CH2OH��l����H��0
��g��+HCl��g��?ClCH2CH2OH��l����H��0| ���������� | ��Է������� | �۵㣨�棩 | �е㣨�棩 |
| �������� | 44 | -112��2 | 10.8 |
| 2-���Ҵ� | 80.5 | -67.5 | 128.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
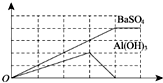 ��֪����ҺQ�еμ���ҺP���������ֳ��������ó��������������P��Һ�������ϵ��ͼ��ʾ����Q��P�ֱ�Ϊ��������
��֪����ҺQ�еμ���ҺP���������ֳ��������ó��������������P��Һ�������ϵ��ͼ��ʾ����Q��P�ֱ�Ϊ��������| A�� | QΪNH4Al��SO4��2��PΪBa��OH��2 | B�� | QΪBa��OH��2��PΪ���� | ||
| C�� | QΪ������PΪBa��OH��2 | D�� | QΪBa��AlO2��2��PΪ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ�鷽����ֻҪ����дѡ���Լ��� | ��1�� | ��2�� |
| AlCl3��Һ��MgCl2��Һ��NaOH��Һ | ��ˮ��NaBr��Һ | |
| ʵ������ | ��Է���ʽ�٢ڻ���Թ��������ɰ�ɫ���������ɫ������ʧ�� ��Է���ʽ�ܣ��Թ����а�ɫ������ | ��Һ��dz����ɫ��ɳȻ�ɫ |
| �йط�Ӧ�����ӷ���ʽ | ��Al3++3OH-�TAl��OH��3�� ��Al��OH��3+OH-�TAlO-2+H2O ���Al3++4OH-�TAlO-2+2H2O ��Mg2++2OH-�TMg��OH��2�� | 2Br-+Cl2�TBr2+2Cl- |
| ���� | �����ԣ�Mg��Al | �ǽ����ԣ�Cl��Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ɫ������ | B�� | �������� | ||
| C�� | �������� | D�� | û���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 24Mg32S �����е�����������������֮��Ϊ1��1 | |
| B�� | CO2��PCl5�����и�ԭ������㶼����8 ���ӽṹ | |
| C�� | ��aXm+��bYn-�������ӵ��Ӳ�ṹ��ͬ����a-b=n-m | |
| D�� | Ԫ�����ڱ��е�4 ��Ԫ���γɵĻ�������Ŀ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com