
【题目】绿矾(FeSO4·7H2O)可作人体补血剂。某同学欲测定补血剂中铁元素的含量,设计了如下实验步骤:

请回答下列问题:
(1)步骤②加入过量H2O2的目的是__。
(2)步骤③加入了足量氨水,反应的离子方程式为__。
(3)步骤④中一系列处理的操作步骤:过滤、__、干燥、灼烧、冷却、称量。
(4)若实验中铁无损耗,则每片补血剂中含铁元素的质量为__g。
(5)另一位同学认为用酸性KMnO4溶液滴定也能进行铁元素含量的测定,①写出酸性KMnO4溶液与Fe2+反应的离子方程式___。
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、药匙、玻璃棒、量筒、烧杯、胶头滴管外,还需__。
③上述实验中的KMnO4溶液需要进行酸化处理,可用于酸化的酸的化学式为__。
【答案】将Fe2+全部氧化为Fe3+ Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ 洗涤 0.07a 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 250mL容量瓶 H2SO4
【解析】
测定补血剂中铁元素的含量,由实验流程可知,研细后加硫酸溶解,过滤分离出不溶性物质,滤液中含Fe2+,加过氧化氢发生反应:2Fe2++H2O2+2H+=2Fe3++2H2O,步骤③加入了足量氨水,发生反应:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+,步骤④中过滤、洗涤、干燥、灼烧、冷却、称量,ag为氧化铁的质量,由于Fe原子守恒可计算含量,酸性高锰酸钾具有强氧化性,可将Fe2+氧化为Fe3+,发生反应:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,配制一定物质的量浓度的KMnO4溶液250mL,一定要选250 mL容量瓶,因为高锰酸钾可氧化氯离子,硝酸具有氧化性均会干扰实验,只有选用硫酸进行酸化。
根据以上分析进行解答。
(1)步骤②加入过量H2O2的目的是将Fe2+全部氧化为Fe3+。
答案为:将Fe2+全部氧化为Fe3+。
(2) 步骤③加入了足量氨水,反应的离子方程式为Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+。
答案为:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+。
(3) 步骤④中一系列处理的操作步骤为:过滤、洗涤、干燥、灼烧、冷却、称量。
答案为:洗涤。
(4) ag为氧化铁的质量,若实验中铁无损耗,由Fe原子守恒可知,每片补血剂中含铁元素的质量为: 。
。
答案为:0.07a。
(5)①酸性高锰酸钾具有强氧化性,可将Fe2+氧化为Fe3+,发生反应:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
②配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、药匙、玻璃棒、量筒、烧杯、胶头滴管外,还需250 mL容量瓶。
答案为:250 mL容量瓶。
③因高锰酸钾可氧化氯离子,硝酸具有氧化性均会干扰实验,实验中的KMnO4溶液需要进行酸化处理,只有选用稀硫酸进行酸化。
答案为:H2SO4 。


科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)![]() H、
H、![]() H、
H、![]() H互为__;O2、O3互为__。
H互为__;O2、O3互为__。
(2)在下列固体中:a.CaCl2 b.KOH c.He d.H2SO4 e.NH4Cl f.金刚石
①其中不含化学键的物质是__。
②既含有离子键又含有共价键的物质是__(填序号)。
(3)如图是几种常见的电池装置。请回答:

①电池Ⅰ中负极反应式是__,溶液中H+向__(填“负”或“正”)极移动,若1mol电子流过导线,则产生氢气的物质的量是__mol。
②电池Ⅱ属于__电池(填“一次”或“二次”).
③电池Ⅲ是氢氧燃料电池,写出负极的电极反应式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是

A. Ka=1×10-6
B. b点时,c(B+)=c(A-)
C. c点时,![]() 随温度升高而增大
随温度升高而增大
D. a→c过程中水的电离程度始终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与完成相关实验问题讨论。
(实验目的)制取乙酸乙酯
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:

根据分析回答:(1)三位同学设计的装置中最不合理的是____(选填“甲”或“乙”或“丙”),原因是_________________。
(实验步骤)
a.按所选择的装置组装仪器,在试管①中先加入3mL乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;
c.在试管②中加入适量的饱和Na2CO3溶液;
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象时停止实验。
(2)试管①中加入浓硫酸的作用是______________________________
(3)该实验中长导管的作用是___________________。
(4)试管②中饱和Na2CO3溶液的作用是_______________;可否用NaOH溶液代替Na2CO3溶液?_____(填“是”或“否”),理由是用化学方程式回答_______________。
(5)写出试管①中乙醇工业制取的化学方程式________________________________;
II.实验室制备硝基苯的主要步骤如下:
a、配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b、向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c、在55~60℃下发生反应,直至反应结束;
d、除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;
e、将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。请填写下列空白:
①制备硝基苯的反应类型是________________。
②配制一定比例的浓H2SO4与浓HNO3的混合酸时,操作的注意事项是:_____。
③步骤d中洗涤、分离粗硝基苯应使用的仪器是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究铜和浓硫酸的反应,下列装置或操作错误的是( )
A.上下移动装置甲中的铜丝体现绿色化学的思想
B.装置乙可用于收集SO2气体
C.将试管中的液体倒入装置丙中稀释,观察颜色可确定CuSO4的生成
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO4·5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)甲基的电子式___________。
(2)有下列六组物质:属于同系物的是______,属于同分异构体是______,属于同种物质的是______。(填序号)
A. 与
与 B.
B.![]() 与
与![]()
C.![]() 与
与![]() D.
D.![]() 与
与![]()
E.ClC(CH3)3与(CH3)2CHCH2Cl F.![]() 与CH3﹣CH2Cl.
与CH3﹣CH2Cl.
(3)写出由甲苯制备TNT的化学反应方程式___________。
(4)相对分子质量为72且只有一种一氯代物的烷烃的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为500℃时,反应4NH3+5O2![]() 4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为 ( )
4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为 ( )
A.v(O2)=0.01mol/(Ls)B.v(NO)=0.08mol/(Ls)
C.v(H2O)=0.0013mol/(Ls)D.v(NH3)=0.002mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用废铁屑制备磁性胶体粒子,制取过程如下:

下列说法不正确的是
A. 用Na2CO3溶液浸泡是为了除去废铁屑表面的油污
B. 通入N2是防止空气中的O2氧化二价铁元素
C. 加适量的H2O2是为了将部分Fe2+氧化为Fe3+,涉及反应:H2O2+2Fe2++2H+=2Fe3++2 H2O
D. 溶液A中Fe2+和Fe3+的浓度比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
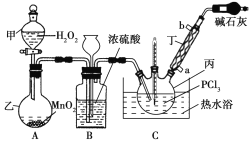
已知PCl3和三氯氧磷的性质如表:
熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65 ℃,原因是________。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com