
【题目】下列反应的离子方程式正确的是( )
A.NaHCO3与足量Ca(OH)2的反应: 2HCO3-+Ca2++2OH-=CaCO![]() ↓+CO32-+2H2O
↓+CO32-+2H2O
B.少量Na投入冷水中;Na+2H2O=Na++OH-+H2↑
C.CuSO4与Ba(OH)2的反应: Cu2++ SO42-+Ba2++2OH![]() =Cu(OH)2↓+BaSO4↓
=Cu(OH)2↓+BaSO4↓
D.AlCl3溶液中加入足量氨水:Al3++4OH![]() =AlO2-+2H2O
=AlO2-+2H2O
【答案】C
【解析】
A.NaHCO3与足量Ca(OH)2的反应生成碳酸钙沉淀、氢氧化钠和水,反应的离子方程式为:HCO3-+Ca2++OH-=CaCO3↓+H2O,故A错误;
B.少量Na投入冷水中生成氢氧化钠和氢气,反应的离子方程式为;2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.CuSO4与Ba(OH)2的反应生成硫酸钡和氢氧化铜沉淀,反应的离子方程式为:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓,故C正确;
D.AlCl3溶液中加入足量氨水生成氢氧化铝沉淀和氯化铵,氨水不能溶解生成的氢氧化铝,反应的离子方程式为:Al3++3NH3H2O=Al(OH)3↓+3NH4+,故D错误;
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(化学——选修5:有机化学基础)(15分)
有机化合物G是合成维生素类药物的中间体,其结构简式如图所示

G的合成路线如下图所示:

其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:
请回答下列问题:
(1)G的分子式是 ,G中官能团的名称是 ;
(2)第②步反应的化学方程式是 ;
(3)B的名称(系统命名)是 ;
(4)第②~⑥步反应中属于取代反应的有 (填步骤编号);
(5)第④步反应的化学方程式是 ;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式 。
①只含一种官能团;②链状结构且无-O-O-;③核磁共振氢谱只有2种峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室制得气体中常含有杂质,影响其性质检验。下图A为除杂装置,B为性质检验装置,完成下列表格:
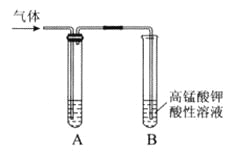
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | _________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是________________。 | NaOH溶液 |
③ | 乙炔 | 电石与饱和食盐水反应 | _________ |
Ⅱ.为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
试管编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是_____________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是________________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。
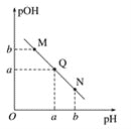
图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学配制一定物质的量浓度的NaOH溶液时,造成所配制溶液浓度偏高的原因是( )
A. 转移时容量瓶未干燥
B. 定容时俯视刻度线
C. 没有洗涤烧杯和玻璃棒
D. 用带游码的托盘天平称2.4 g NaOH时误用了“左码右物”方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质。

请回答下列问题:
(1)通过试管乙中发生的____现象,说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有______性。
(2)若要收集试管甲中生成的气体,可以采用_________方法收集(填序号)。
①排水取气法 ② 向上排空气取气法 ③ 向下排空气取气法
(3)写出试管甲中所发生反应的化学反应方程式__________。
(4)试管乙口部浸有碱液的棉花的作用是__________,此防范措施也说明产生的气体是 ______气体(填“酸性”、“中性”或“碱性”),_______(填“有”或“无”)毒性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A. 在![]() 分子中含有1个手性C原子
分子中含有1个手性C原子
B. 氢键是一种特殊化学键,它广泛地存在于自然界中
C. 碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子
D. 含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 室温下用稀NaOH溶液吸收Cl2:Cl2+2OH![]() ClO+Cl+H2O
ClO+Cl+H2O
B. 用铝粉和NaOH溶液反应制取少量H2:Al+2OH![]()
![]() +H2↑
+H2↑
C. 室温下用稀HNO3溶解铜:Cu+2![]() +2H+
+2H+![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com