
 .反应中氧化剂与还原剂的物质的量之比为5:2.
.反应中氧化剂与还原剂的物质的量之比为5:2.分析 (1)最高价态的元素只有氧化性,最低价态的元素只有还原性,中间价态的元素既有氧化性又有还原性,据此分析解答;
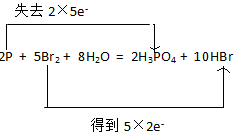
(2)2P+5Br2+8H2O=2H3PO4+10HBr,P元素化合价由0价升高到+5价,则P为还原剂,Br2中Br元素化合价由0价降低到-1价,则Br2为氧化剂,转移电子数为10e-,据此分析;
(3)在反应3S+6KOH=2K2S+K2SO3+3H2O中,只有S元素的化合价发生变化,S→K2S,化合价降低为氧化剂,S→K2SO3,化合价升高为还原剂,据此分析.
解答 解:(1)Fe3+、Mg2+、H+中的化合价都是最高价态,所以都只有氧化性;
S2-、I-中的化合价都是最低价态,所以都只有还原性;
Fe2+、S中的化合价是中间价态,所以既有氧化性又有还原性,
故答案为:H+、Mg2+、Fe3+;S2-、I-;Fe2+、S;
(2)2P+5Br2+8H2O=2H3PO4+10HBr,P元素化合价由0价升高到+5价,则P为还原剂,Br2中Br元素化合价由0价降低到-1价,则Br2为氧化剂,转移电子数为10e-,则表示出反应中电子转移的方向和数目为 ,反应中氧化剂与还原剂的物质的量之比为5:2;故答案为:
,反应中氧化剂与还原剂的物质的量之比为5:2;故答案为: ;5:2;
;5:2;
(3)在反应3S+6KOH=2K2S+K2SO3+3H2O中,只有S元素的化合价发生变化,氧化剂和氧化剂都是S,
反应中S→K2S,S化合价降低,则S为氧化剂,K2S为还原产物;
S→K2SO3,S化合价升高,则S为还原剂,K2SO3为氧化产物;
反应的离子方程式为:3S+6OH-=2S2-+SO32-+3H2O;
故答案为:K2SO3;K2S;3S+6OH-=2S2-+SO32-+3H2O.
点评 本题考查氧化还原反应概念与计算,难度不大,根据化合价判断氧化剂与还原剂、还原产物与氧化产物是关键,明确元素化合价与氧化性和还原性的关系是解本题关键,难度不大.


科目:高中化学 来源: 题型:实验题
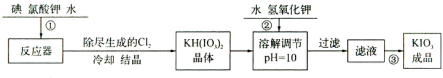
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液 | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL0.1mol•L-1KI溶液,振荡 | 溶液无变化 |
| 然后再滴入1mol•L-1的H2SO4,充分振荡 | 溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| C. | S(s)+O2(g)═SO2(g);△H=+269.8kJ/mol(反应热) | |
| D. | 2HCl(g)═Cl2(g)+H2(g);△H=-184.6kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75%酒精 | B. | 氢氧化铁胶体 | C. | 硝酸钠 | D. | 粗盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都具有很高的熔点 | |
| B. | 最外层电子数少于 3 个的都是金属 | |
| C. | 都能导电、传热 | |
| D. | 都只能和酸不能和碱发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用手掰开一块金属钠,观察钠的颜色 | |
| B. | 钠投入硫酸铜溶液中,既有气体又有沉淀生成 | |
| C. | 氧化钠和过氧化钠可用作潜艇里氧气的来源 | |
| D. | 氧化钠和过氧化钠与二氧化碳反应的产物完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com