
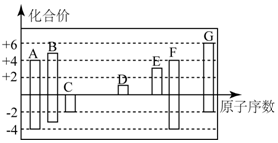
 ��ͼ�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵ��
��ͼ�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵ�� ����������ѧ������Ϊ���Ӽ��ͷǼ��Լ���
����������ѧ������Ϊ���Ӽ��ͷǼ��Լ������� ������Ԫ���У�A��F����+4��-4�ۣ����ڢ�A�壬��ԭ������A��F����AΪ̼��FΪSi��C��G����-2�ۣ���G��+6��G��ԭ�������ϴ�CΪOԪ�ء�GΪSԪ�أ�B��+5��-3�ۣ�ԭ����������̼����֮�䣬��BΪNԪ�أ�D��+1�ۣ�E��+3�ۣ��ֱ��ڢ�A�塢��A�壬ԭ������������D��E��Si����DΪNa��EΪAl�����Ԫ�������ɡ�λ���Խ��⣮
��� �⣺������Ԫ���У�A��F����+4��-4�ۣ����ڢ�A�壬��ԭ������A��F����AΪ̼��FΪSi��C��G����-2�ۣ���G��+6��G��ԭ�������ϴ�CΪOԪ�ء�GΪSԪ�أ�B��+5��-3�ۣ�ԭ����������̼����֮�䣬��BΪNԪ�أ�D��+1�ۣ�E��+3�ۣ��ֱ��ڢ�A�塢��A�壬ԭ������������D��E��Si����DΪNa��EΪAl��
��1��Ԫ��BΪN�������ڱ��е�λ�ã��ڶ����ڢ�A�壬�䵥��ΪN2�������ڴ��ڵ����������ṹʽΪN��N��
�ʴ�Ϊ���ڶ����ڢ�A�壻N��N��
��2��Na2O2Ϊ���ӻ��������к������Ӽ��ͷǼ��Թ��ۼ��������ʽΪ ��
��
�ʴ�Ϊ�� �����Ӽ��ͷǼ��Լ���
�����Ӽ��ͷǼ��Լ���
��3�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶ԽС�������Ӱ뾶��С˳���ǣ�S2-��O2-��Na+��
�ʴ�Ϊ��S2-��O2-��Na+��
��4��C��G���⻯��ֱ�ΪH2O��H2S��H2O����֮���γ�������е��������ģ�����Ԫ�صķǽ����Ա���Ԫ��ǿ�����ȶ��ԣ�H2O��H2S��
�ʴ�Ϊ��H2S������
��4��D��E������������ˮ����ֱ�ΪNaOH��Al��OH��3�����߷�����Ӧ����ƫ�����ƺ�ˮ�����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ؼ��Ǹ��ݻ��ϼ���ԭ�������ƶ�Ԫ�أ�ע���Ԫ�������ɵ��������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� 0.1 mol ������ܽ��� 1 L ˮ�� | |
| B�� | �� 10 g ��������Ϊ 98%�������� 990 g ˮ��� | |
| C�� | �� 8 g ������������ˮ����� 1 L ��Һ | |
| D�� | �� 0.1 mol ����������ˮ����� 1L ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
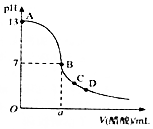 298Kʱ����20mLbmol•L-1����������Һ�е���0.10mol•L-1�Ĵ��ᣬ��Һ��pH�����Ӵ���������ϵ��ͼ��ʾ�������й�������ȷ���ǣ�������
298Kʱ����20mLbmol•L-1����������Һ�е���0.10mol•L-1�Ĵ��ᣬ��Һ��pH�����Ӵ���������ϵ��ͼ��ʾ�������й�������ȷ���ǣ�������| A�� | a��20 | |
| B�� | C����Һ�У�c��CH3COO-��+c��CH3COOH��=c��Na+�� | |
| C�� | A��B��C��D�ĵ�ˮ�ĵ���̶ȴ�С˳��Ϊ��D��B��C��A | |
| D�� | ����ĵ���ƽ�ⳣ��Ka=2.0��10-7/��0��la-2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4��NaOH--��ʴƷ | B�� | CH4--��ȼҺ�� | ||
| C�� | Na--��ʪ��ȼ��Ʒ | D�� | KMnO4--������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O | B�� | CO2 | C�� | N2O | D�� | CH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѡ�� | ��ʵ�� | ������ | ������ |
| ��A | �������Һ�м���ϡH2SO4�����ȼ����ӣ���ȴ���ټ�������Cu��OH��2��Һ������������ | û��ש��ɫ�������֡� | ����û��ˮ��������� |
| ��B | ����ij��Һ�еμ�BaCl2��Һ������ϡ�����ữ | ��Һ�в�����ɫ��������ϡ����ܽ⡡ | ԭ��Һ��һ����Ag+�� |
| ��C | ����ϡ�����ữ��H2O2��Һ����Fe��NO3��2��Һ�� | ��Һ���ɫ | �����ԣ�H2O2��Fe3+ǿ |
| ��D | �����з�̪��Na2CO3��Һ�м�������BaCl2���� | ��Һ��ɫ��dz�� | ֤��Na2CO3��Һ�д���ˮ��ƽ�⡡ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
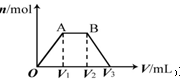 ��KOH��Ca��OH��2�Ļ����Һ��C��OH-���T0.1mol•L-1��ȡ����Һ500mL��������ͨ��CO2��ͨ��CO2�������V�������ɳ��������ʵ�����n���Ĺ�ϵ��ͼ��ʾ��ͼ�У�V1��Ϊ112mL����״��������ͼ��V2��V3���������λΪmL���ֱ��ǣ�������
��KOH��Ca��OH��2�Ļ����Һ��C��OH-���T0.1mol•L-1��ȡ����Һ500mL��������ͨ��CO2��ͨ��CO2�������V�������ɳ��������ʵ�����n���Ĺ�ϵ��ͼ��ʾ��ͼ�У�V1��Ϊ112mL����״��������ͼ��V2��V3���������λΪmL���ֱ��ǣ�������| A�� | 560��672 | B�� | 1008��1120 | C�� | 2240��2352 | D�� | 392��504 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com