
| A. | KC1 | B. | SiO2 | C. | SO3 | D. | NaOH |
分析 化学式能真实表示物质分子组成的是分子晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体,据此进行判断.
解答 解:A.KC1为离子化合物,只有钾离子和氯离子,没有分子,故A错误;
B.Si02为原子晶体,是由硅原子和氧原子以共价键构成的空间网状结构,没有Si02分子,故B错误;
C.SO3为非金属氧化物,属于分子晶体,晶体中只存在分子,能用SO3能表示物质分子组成,故C正确;
D.NaOH为离子化合物,只有钠离子和氢氧根离子,没有分子,故D错误;
故选C.
点评 本题考查物质组成与化学式的关系,题目难度不大,试题侧重于学生的分析能力的考查,掌握常见物质晶体类型及常见分子晶体是解答的关键.


科目:高中化学 来源: 题型:选择题
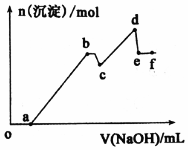 已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )
已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )| A. | b 点沉淀-Al(OH)3;d 点沉淀-A1(OH)3和Mg(OH)2;e点溶质-NaA1O2 | |
| B. | 依据题意,用NaOH不能完全分离Mg2+和Al3+离子 | |
| C. | cd 段发生的反应为:Mg2++2OH-=Mg(OH)2↓ | |
| D. | bc 段发生的反应为:Al(OH)3+OH-=A1O2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +R3
+R3 $\stackrel{C_{2}H_{5}ONa}{→}$
$\stackrel{C_{2}H_{5}ONa}{→}$ +R2OH
+R2OH .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 将气体X分别通入溴水和酸性高锰酸钾溶液中,两溶液均褪色 | 气体X一定是C2H4 |
| B | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32--强 |
| C | 向某溶液中先滴加少量氯水,再滴加2滴KSCN溶液,溶液变成血红色 | 原溶液中一定含有Fe2+ |
| D | 将H2S气体通入浓度均为0.01mol•L-l的ZnSO4和CuSO4混合溶液中,先出现CuS黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有人称“一带一路”是“现代丝绸之路”,丝绸的主要成分是纤维素,属于天然高分子化合物 | |
| B. | 陶瓷、水泥和玻璃都属于硅酸盐产品 | |
| C. | 废旧钢材焊接前,可依次用饱和Na2CO3溶液、饱和NH4Cl溶液处理焊点 | |
| D. | 使用可降解的聚碳酸酯塑料和向燃煤中加入生石灰,都能减轻环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
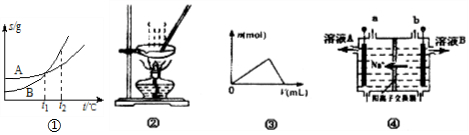
| A. | 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
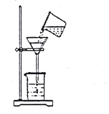
| B. | 用图②所示装置蒸发FeCl3溶液制备无水FeCl3 | |
| C. | 图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化 | |
| D. | 图④电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
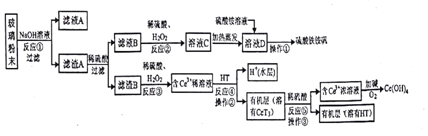
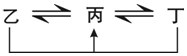 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系: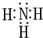 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com