
| A. | 溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO-) | |
| B. | 溶液①、②等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| C. | 溶液①、③等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=c(Na+) | |
| D. | 溶液①、③等体积混合,混合液中c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
分析 A.溶液①、②等体积混合,二者恰好反应生成0.05mol/L的CH3COONa;
B.溶液①、②等体积混合,二者恰好反应生成0.05mol/L的CH3COONa,根据物料守恒判断;
C.溶液①、③等体积混合,CH3COOH电离程度大于CH3COO-水解程度导致溶液呈酸性,溶液中存在物料守恒,根据物料守恒判断;
D.溶液①、③等体积混合,CH3COOH电离程度大于CH3COO-水解程度导致溶液呈酸性,但CH3COOH电离程度较小.
解答 解:A.溶液①、②等体积混合,二者恰好反应生成0.05mol/L的CH3COONa,两种溶液中醋酸根离子都水解但水解程度较小,所以混合液中c(CH3COO-)小于溶液③中的c(CH3COO-),故A错误;
B.溶液①、②等体积混合,二者恰好反应生成0.05mol/L的CH3COONa,混合溶液体积是原来①或②的2倍,所以浓度是原来的一半,根据物料守恒得c(CH3COO-)+c(CH3COOH)=0.05mol/L,故B错误;
C.溶液①、③等体积混合,CH3COOH电离程度大于CH3COO-水解程度导致溶液呈酸性,溶液中存在物料守恒,根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c(Na+),故C错误;
D.溶液①、③等体积混合,CH3COOH电离程度大于CH3COO-水解程度导致溶液呈酸性,但CH3COOH电离程度较小,所以c(CH3COO-)>0.05mol/L、c(Na+)=0.05mol/L、c(CH3COOH)<0.05mol/L但大于c(H+),则离子浓度大小顺序是c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,明确混合溶液中溶质成分及其性质是解本题关键,侧重考查学生分析判断能力,注意:溶液等体积混合后溶液浓度的变化,为易错点.


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:填空题
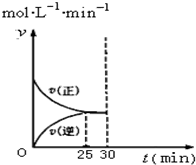 实验室模拟SO2与O2在一定条件下反应生成SO3.现将1.00mol SO2与1.00mol O2置于一体积不变的1L密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-l.在其他条件不变的情况下,不同温度时SO3的浓度(mol•L-1)随时间(min)的变化如表格所示:
实验室模拟SO2与O2在一定条件下反应生成SO3.现将1.00mol SO2与1.00mol O2置于一体积不变的1L密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-l.在其他条件不变的情况下,不同温度时SO3的浓度(mol•L-1)随时间(min)的变化如表格所示:  | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| T1 | 0 | 0.20 | 0.30 | 0.39 | 0.47 | 0.50 | 0.50 |
| T2 | 0 | 0.25 | 0.40 | 0.40 | 0.40 | 0.40 | 0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 碳酸氢钠与盐酸反应:CO32-+2 H+═CO2↑+H2O | |
| C. | 硫酸镁溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 少量CO2通入澄清石灰水中:CO2+Ca2++2OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
| 原料生产工艺过程 | |
| 乙炔 | CaCO3$\stackrel{催化剂/△}{→}$CaO$→_{1100℃}^{②+C、电炉}$CaC2$\stackrel{③饱和食盐水}{→}$C2H2 |
| 乙烯 | 来源于石油裂解气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | TiCl4溶于大量水加热制备TiO2 | |
| B. | FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 | |
| C. | 配制氯化亚铁溶液时需加少量铁粉 | |
| D. | 将氯化铝溶液加热蒸干并灼烧,最后得到的固体是氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{14}$C的中子数是8 | |
| B. | ${\;}_{6}^{14}$C与${\;}_{6}^{12}$C互为同位素 | |
| C. | ${\;}_{6}^{14}$C转化为${\;}_{6}^{12}$C不是化学变化 | |
| D. | ${\;}_{6}^{14}$C与${\;}_{6}^{12}$C互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 葡萄可用于酿酒.
葡萄可用于酿酒. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.| ①称取E4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①有机物E的相对分子量为90: |
| ②将此9.0gE在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). | ②9.0g有机物E完全燃烧时,经计算:生成CO2共为0.3 mol, 生成的H2O5.4g. 有机物E的分子式C3H6O3 |
| ③经红外光谱测定,证实其中含有羟基,羧基,甲基; | ③E的结构简式CH3CH(OH)COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物在滤液中 | B. | 杂质在滤液中 | C. | 有机物滤纸上 | D. | 杂质在溶剂中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com