
设NA代表阿伏加德罗常数的值。下列有关叙述正确的是 ( )
A.分子数为NA的CO、C2H4混合气体的体积约为22.4 L,质量为28 g
B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中NH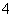 和NO
和NO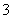 的总数为0.2NA
的总数为0.2NA
C.标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
D.1 mol甲基(—CH3)所含的电子数为9NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
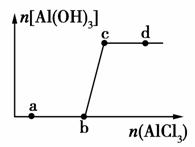
A.a点对应的溶液中:Na+、Fe3+、SO 、HCO
、HCO
B.b点对应的溶液中:Ag+、Ca2+、NO 、F-
、F-
C.c点对应的溶液中:Na+、S2-、SO 、Cl-
、Cl-
D.d点对应的溶液中:K+、NH 、I-、CO
、I-、CO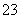
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的 金属,相关物质间的关系如下图所示。
金属,相关物质间的关系如下图所示。
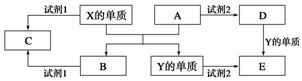
(1)X的单质与A反应的化学方程式是_______________________________________。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 ________________________________________________________________
________________________________________________________________ ________。
________。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是_____________________________________
________________________________________________________________________。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)________________________________________________________________________。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
N0为阿伏加德罗常数的值。下列叙述正确的是 ( )
A.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0
B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0
C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下有:①6.72 L CH4,②3.01×1023个HCl分子,③13.6 g H2S,④0.2 mol NH3。下列对这四种气体的描述正确的是 ( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abc B.bcd C.abd D.abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计如图所示的装置分别进行不同的探究实验(夹持装置已略去),请回答下列问题:

| 实验 | 药品 | 制取气体 | 量气管中液体 |
| Ⅰ | Cu、稀HNO3 | NO | H2O |
| Ⅱ | NaOH(s)、浓氨水 | NH3 | |
| Ⅲ | 电石、饱和NaCl溶液 | C2H2 | H2O |
| Ⅳ | 镁铝合金、NaOH溶液 | H2 | H2O |
(1)如何检验如图所示装置的气密性:________________________________________。
(2)该同学认为实验Ⅰ可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?__________(填“可行”或“不可行”),原因是_______________________。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是____________________________________,
打开开关K,产生的气体经验纯后点燃,现象是______________________________。
(4)实验Ⅱ中量气管中的液体最好是________(填字母编号,下同)。
a.浓NaOH溶液 b.氨水
c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需要吸收处理。以下各种尾气吸收装置中,适用于吸收NH3,而且能防止倒吸的有____________________________________________________________。


(5)本实验需对量气管进行多次读数,读数时应注意:①将实验装置恢复到室温,②__________________,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况下的体积,忽略滴入的液体体积对气体体积的影响):
| 编号 | 镁铝合金 质量 | 量气管 第一次读数 | 量气管 第二次读数 |
| ① | 1.0 g | 350.0 mL | 13.7 mL |
| ② | 1.0 g | 350.0 mL | 25.0 mL |
| ③ | 1.0 g | 350.0 mL | 14.3 mL |
根据表中数据,可计算出镁铝合金中铝的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式错误的是
A.Fe(OH)2溶液中加入HNO3溶液:Fe(OH)2+2H+=2H2O+Fe2+
B.盐酸除去铜器表面的铜绿:Cu2(OH)2CO3+4H+=3H2O+2Cu2++CO2↑
C.氯气可以降低的SO2的漂白性:SO2+Cl2+2H2O=2Cl—+4H++SO42—
D.CO2通入饱和碳酸钠溶液:CO2+ CO32—+2Na++H2O=2NaHCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
NM—3和D—58是正处于临床试验阶段的小分子抗癌药物,结构如下。关于NM—3和D—58的叙述,正确的是

A. NM—3和D—58互为同分异构体
B. NM—3和D—58都能与溴水反应,反应类型完全相同
C. 两者都能与NaOH溶液反应,且相同物质的量的NM—3和D—58消耗的NaOH的量相同
D. 都能和H2发生加成反应,且相同物质的量的NM—3和D—58最多消耗的H2物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com