
在下面的电子结构中,第一电离能最小的原子可能是( )
A.ns2np3 B.ns2np5 C.ns2np4 D.ns2np6
科目:高中化学 来源: 题型:
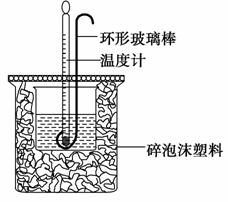
实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
试完成下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是________________________________________________________________
_______________________________________________________________。
不能用铜丝搅拌棒代替环形玻璃棒的理由是_______________________________________________________________。
(2)经数据处理,t2—t1=3.4 ℃。则该实验测得的中和热ΔH=________[盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1________ΔH(填“<”、“>”或“=”),理由是________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是( )
A.Na2O2中阴、阳离子的个数比为1∶1
B.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C.Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D.Na2O2的漂白原理与SO2的漂白原理不同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.原子核外电子在某一时刻的位置可以测定或计算出来
B.原子核外电子的运动轨迹可以描画出来
C.人们常用小黑点的疏密程度来表示电子在原子核外出现概率的大小
D.电子云图中的小黑点表示电子的个数多少
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为短周期元素,A、B同周期,C、D同主族,已知A的阳离子与D的阴离子具有相同的电子层结构,B的阴离子和C的阴离子电子层结构相同,且C离子的核电荷数大于B离子的,则4种元素的电负性顺序正确的是( )
A.A>B>C>D B.D>C>B>A
C.C>D>B>A D.A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
处于相邻两个周期的主族元素A、B、C、D,它们的原子半径依次变小;A离子和B离子的电子层相差两层,且能形成BA2型的离子化合物;C的离子带3个正电荷;D的气态氢化物通式为H2R,D在它的最高价氧化物中的质量分数是40%,原子核中有16个中子。试回答:
(1)写出A、B、C、D的元素符号:
A:________ B:________ C:________ D:________
(2)B、C、D的第一电离能从大到小的顺序如何排列?(写元素符号,下同)______。
(3)A、B、C的电负性从大到小的顺序如何排列?________________________。
(4)向D的氢化物的水溶液中滴入少量A的单质,发生什么现象?___________,写出有关反应的化学方程式:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
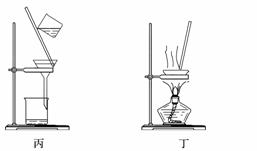
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )
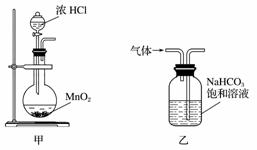
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/ (kJ·mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是__________。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com