
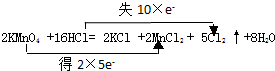 ,
,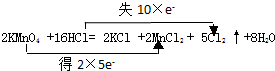 ;
;| 5 |
| 10 |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
| A、冰和干冰既是纯净物又是化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| D、盐酸和食醋既是化合物又是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
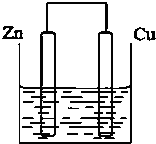 将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.
将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| C | N | O | F | |
| Si | P | S | Cl | |
| Ge | As | Se | Br | |
| Sn | Sb | Te | I | |
| Pb | Bi | Po | At |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水平衡左移 |
| B、增加A,可提高B的转化率 |
| C、平衡后,按起始投料比,再次投入A和B,则A和B的转化率都将增大 |
| D、升温该平衡一定发生移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com