


科目:高中化学 来源: 题型:
| A、H2SO4的摩尔质量是 98 g |
| B、1 mol H2O的质量是 18 g/mol |
| C、Cl-的摩尔质量是 35.5 g/mol |
| D、1 mol N2 的体积是 22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-的水解方程式可表示为:HCO3-+H2O═H3O++CO32- |
| B、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| C、向NaAlO2溶液中通入过量的CO2制Al(OH)3↓2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| D、将16g铁粉投入100mL 4.0mol/L的HNO3溶液中,(还原产物只有NO)3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
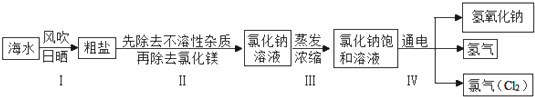

| 阴离子 阳离子 | OH- | CO
| ||
| Ca2+ | 微 | 不 | ||
| Mg2+ | 不 | 微 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2 |
| 步骤二:往步骤一所得溶液中加入适量的 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com