
| A.晶体微粒是分子 | B.干燥或熔化时均能导电 |
| C.晶体内微粒间以范德华力结合 | D.熔点和沸点一般低于原子晶体和离子晶体 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题

 )中含有σ键的数目为_________个。
)中含有σ键的数目为_________个。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | Li | Be | B | C | N | O | F |
| 电负性 | 0.98 | 1.57 | 2.04 | 2.55 | 3.04 | 3.44 | 3.98 |
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| 电负性 | 0.93 | 1.31 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 微粒 | a | b | c | d | e | f | g |
| 原子核数 | 双核 | 双核 | 三核 | 四核 | 四核 | 五核 | 五核 |
| 所带单位电荷 | 0 | -1 | 0 | 0 | +1 | | +1 |
 ④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
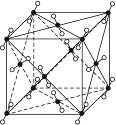
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碘单质的升华和金刚石的熔化 | B.二氧化硅和氯化钾的熔化 |
| C.氧化铝和冰的熔化 | D.乙醇和液氯的汽化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.存在四面体结构单元,O处于中心,Si处于4个顶角 |
| B.最小的环上,有3个Si原子和3个O原子 |
| C.最小的环上,Si和O原子数之比为1:2 |
| D.最小的环上,有6个Si原子和6个O原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com