
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3C≡CH | D. | CH3CH=CHCH3 |
分析 1mol某链烃最多能和1molHCl发生加成反应,则其分子中含有1个C=C键,生成的1mol该卤代烷能和7molCl2发生取代反应,加成时引入1个H原子,所以链烃分子中含有6个H原子,以此来解答.
解答 解:1mol某链烃最多能和1molHCl发生加成反应,则该烃分子含有1个C=C键,
根据1mol生成的该卤代烷能和7molCl2发生取代反应,说明该卤代烃中含有7个H,由于加成时引入1个H原子,则该链烃分子中含有6个H原子,应该为丙烯,结构简式为:CH3CH=CH2,
故选B.
点评 本题考查了有机物结构与性质,题目难度中等,明确加成反应和取代反应原理为解答关键,注意熟练掌握常见有机物结构与性质,试题培养了学生的分析能力及灵活运用能力.


科目:高中化学 来源: 题型:选择题
| A. | NH4+ K+ Na+ CO32- NO3- | B. | K+ Na+ Fe2+ SO42- NO3- | ||
| C. | NH4+ K+ Na+ HCO3-[Al(OH)4]- | D. | NH4+ K+ Na+ NO3- I- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 、-COOH
、-COOH ,D的结构简式
,D的结构简式 .
.

 的同分异构体有多种,写出同时满足:
的同分异构体有多种,写出同时满足: (任写两种).
(任写两种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的水溶液显酸性:H2CO3?2H++CO32- | |
| B. | 氨水中滴入酚酞,溶液变红:NH3•H2O?NH4++OH- | |
| C. | 加热增强纯碱溶液去污能力:CO32-+H2O?HCO3-+OH- | |
| D. | 向AgCl悬浊液中加入Na2S溶液,有黑色沉淀生成:2AgCl+S2-?Ag2S+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 云、水银、CHCOOH、CH3COONa | B. | 稀H2SO4、硫磺、NH3、NaHPO4 | ||
| C. | 空气、苛性钠、HCN、NaH2PO2 | D. | 有色玻璃、液溴、H2SO4、小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
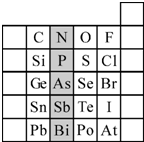


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com