
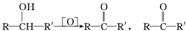 ���ױ�����������
���ױ�����������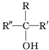 ���ױ�������ȩ��ͪ
���ױ�������ȩ��ͪ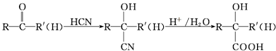
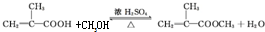 ��
��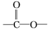 ���ṹ�Ĺ���6�֣�
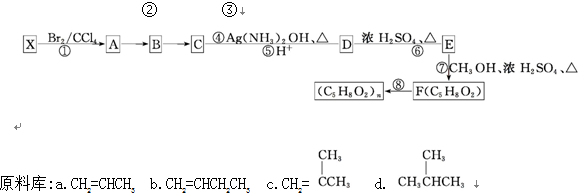
���ṹ�Ĺ���6�֣����� �ɷ�Ӧ��֪X�к���˫������AΪ����������ɷ�Ӧ�ܡ��ݡ���֪B�к�2���ǻ���C�к���һ��ȩ����һ���ǻ���D�к���һ���Ȼ���һ���ǻ���E�к���һ��˫����һ���Ȼ��������֪2��֪X�ĽṹΪ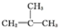 ����AΪ
����AΪ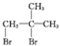 ��BΪ
��BΪ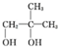 ��CΪ
��CΪ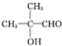 ��DΪ
��DΪ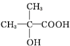 ��EΪ
��EΪ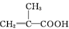 ��
��
FΪ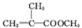 ���Դ˽��1������3����
���Դ˽��1������3����
��4��C�ĽṹΪ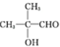 ���칹���к���
���칹���к���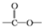 �ṹ�Ŀ������������
�ṹ�Ŀ������������
��5�������֪�ۼ�ȩ��ͪ����������ӳɺ��ữ�ɵñ�ԭ���ʶ�һ��C���ᣬ��ϩ��HBr�ӳɿ�������������CH3CHBrCH3��CH3CH2CH2Br�����е�һ�ֽṹ��ˮ�⡢�����ɱ�ͪ������HCN�ӳɡ��ữ�ɵ�D���ʣ��ڶ��ֽṹ��ˮ�⡢�����õ���ȩ������HCN�ӳɡ��ữ�ɵ�CH3CH2CH��OH��COOH��
��� �⣺��1��X�к���˫����������������֪Ϊ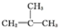 ���ʴ�Ϊ��c��
���ʴ�Ϊ��c��
��2���ڵķ�Ӧ������NaOHˮ��Һ�����ȣ���ķ�Ӧ�����ǼӾ۷�Ӧ��DΪ �������ŵ�����Ϊ�Ȼ����ǻ���
�������ŵ�����Ϊ�Ȼ����ǻ���
�ʴ�Ϊ��NaOHˮ��Һ�����ȣ��Ӿ۷�Ӧ���Ȼ����ǻ���
��3���ߵĻ�ѧ����ʽ��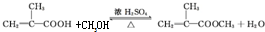 ��
��
�ʴ�Ϊ��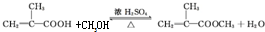 ��
��
��4��C�ĽṹΪ ���칹���к���
���칹���к���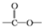 �ṹ�Ŀ���������������������Ϊ���ᡢ2-�����������Ϊ�����������������������������������������6�֣��ʴ�Ϊ��6��
�ṹ�Ŀ���������������������Ϊ���ᡢ2-�����������Ϊ�����������������������������������������6�֣��ʴ�Ϊ��6��
��5����ϩ��HBr�ӳɿ�������������CH3CHBrCH3��CH3CH2CH2Br�����е�һ�ֽṹ��ˮ�⡢�����ɱ�ͪ������HCN�ӳɡ��ữ�ɵ�D���ʣ��ڶ��ֽṹ��ˮ�⡢�����õ���ȩ������HCN�ӳɡ��ữ�ɵ�CH3CH2CH��OH��COOH����M���ܵĽṹ��ʽ��CH3CH2CH��OH��COOH��
�ʴ�Ϊ��CH3CH2CH��OH��COOH��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬���չ����ŵı仯��̼���仯���л���ӦΪ���Ĺؼ������ط������ƶ������Ŀ��飬ע��ϰ������Ϣ���л������ʵ�Ӧ�ã���Ŀ�ѶȲ���


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a=+90.3 | |
| B�� | ���º�ѹ�£����Ѵ�ƽ��ķ�ӦI��ϵ���ٳ�������Heʱƽ�������ƶ� | |
| C�� | �����������䣬��ѹ�Է�Ӧ��ķ�Ӧ������Ӱ�� | |
| D�� | �����������䣬�����¶ȿ���߷�Ӧ����CO2��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�Cu-Znԭ����У���������1.12LH2ʱ��ת�Ƶĵ�����ӦС��0.1NA | |
| B�� | 1molSO2������O2��һ�������·�Ӧ����SO2����ת��2NA������ | |
| C�� | 2.1gDTO������������ΪNA | |
| D�� | ���³�ѹ�£�28gC2H4��CO�Ļ�������к���̼ԭ�ӵ���ĿΪ1.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
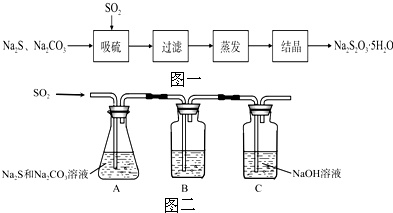
| ��� | ʵ����� | Ԥ������ | ���� |
| �� | ȡ������Ʒ���Թ��У�������������ˮ��������ܽ⣬�μ�����ϡ���ᣬ�ٵμ�����AgNO3��Һ���� | �а�ɫ�������� | ��Ʒ��NaCl |
| �� | ��ȡ������Ʒ���ձ��У�������������ˮ����ֽ����ܽ⣬�������CaCl2��Һ�����裬���ã���pH�Ʋⶨ�ϲ���ҺpH�� | �а�ɫ�������ɣ��� ����ҺpH��10.2 | ��Ʒ��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1Lˮ�к���1molH2SO4 | |
| B�� | 1L��Һ�к���1molH+ | |
| C�� | ��98gH2SO4����1Lˮ�����������Һ | |
| D�� | 1L������Һ�к���96gSO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��������ԭ��֮�䣬Ҳ�����ڷ���֮�� | |
| B�� | ���Ӽ�������������֮��������� | |
| C�� | ���ӻ�������Ժ����ۼ� | |
| D�� | ���Ӽ�������Խ����Խ�ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
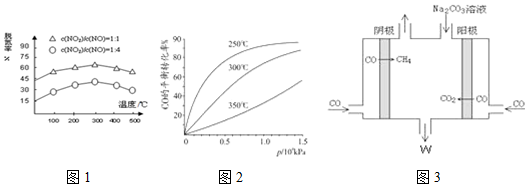
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com