
【题目】Zn+![]() +OH-+H2O―→NH3↑+
+OH-+H2O―→NH3↑+![]() 配平后,离子方程式中H2O的化学计量数是( )
配平后,离子方程式中H2O的化学计量数是( )
A. 2 B. 4 C. 6 D. 8
科目:高中化学 来源: 题型:
【题目】如图是石蜡油在炽热碎瓷片的作用下产生C2H4,并检验C2H4性质的实验,完成下列各题。

(1)B 中溶液褪色,原因是______________
(2)C 中反应的化学方程式为_____________
(3)在D 处点燃时必须进行的操作是___________,D 处反应的化学方程式为______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g)+nB(g)![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是

A. T1>T2,p1>p2,m+n>r,正反应吸热
B. T1<T2,p1<p2,m+n<r,正反应吸热
C. T1>T2,p1>p2,m+n<r,正反应放热
D. T1<T2,p1<p2,m+n>r,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:S(g) + O2 (g) = SO2(g) ΔH=-Q1kJ/mol ; S(s) + O2 (g) = SO2(g) ΔH=-Q2 kJ/mol。 则Q1 Q2
A. 大于 B. 小于 C. 等于 D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

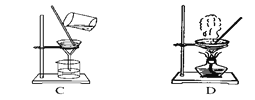
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);
(2)除去自来水中的Cl-等杂质,选择装置A,装置A中①的名称是________,进水的方向是从________口进水。实验时A中除加入少量自来水外,还需加入少量碎瓷片的作用是________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补 B.冷却后补加 C.不需补加 D.重新配料
收集完蒸馏水后,是先撤酒精灯还是先停冷凝水?_________________________。A中不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(3)①从碘水中分离出I2,可以选择以下哪种萃取剂_____________;
A.酒精 B.苯 C.汽油 D.食盐水
②该分离方法的名称为________。
③分液漏斗在使用前须清洗干净并________;
④在选择以上萃取剂时,本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。装置B在分液时为使液体顺利滴下,除打开旋塞外,还应进行的具体操作是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在科研与生活中有很重要的作用。回答下列问题:
(1)碘可用作心脏起搏器电源——锂碘电池的材料,则碘电极是电池的______(填“正”或“负”)极。
(2)“加碘食盐”中含有少量的KIO3,向其中加入亚硫酸氢钠溶液,能产生使淀粉变蓝的物质,则该反应中氧化剂与还原剂的物质的量之比是_______________。
(3)碘单质与氢气反应的能量变化过程如图所示:

写出碘I2(s)转化成碘I2(g)的热化学方程式:__________________________________。
(4)在合成氨工业中用I2O5来测定CO的含量:5CO(g)+I2O5(s) ![]() 5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数
5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数![]() (CO)随时间t的变化曲线如图所示。回答下列问题:
(CO)随时间t的变化曲线如图所示。回答下列问题:
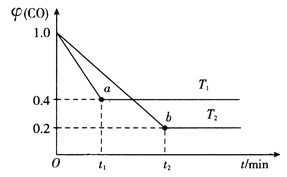
①温度T1下的平衡转化率![]() =________%,b点的平衡常数K2=__________。
=________%,b点的平衡常数K2=__________。
②在温度T2下,反应达到平衡后再充入适量的CO,重新达到平衡时;CO气体的转化率将_______(填“变大”“变小”或“不变”),该反应的△H_____(填“>”“<"或“=”)0。
③下列各种措施能提高该反应的CO转化率的是____________。
A.升温 B.加压 C.添加催化剂 D.移走部分CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四组分散系:①汽油和水形成的乳浊液、②含有泥沙的食盐水、③溶有碘(I2)的碘化钾溶液、④乙二醇和丙三醇混合溶液(乙二醇和丙三醇的部分物理性质见下表)。

请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )

A. ①﹣(3)﹣分液
B. ②﹣(2)﹣过滤
C. ③﹣(2)﹣萃取
D. ④﹣(1)﹣蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设一个蛋白质分子是由二条肽链共500个氨基酸分子组成,则此蛋白质分子中-COOH数目至少为( )
A. 2个 B. 501个 C. 502个 D. 1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g液态甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧的热化学方程式为________________________________________________。
(2)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量,则表示该反应的热化学方程式为_______________________。
Ⅱ.(1)下列事实能用化学平衡移动来原理解释的是 _________
A.打开冰啤酒瓶盖,看到瓶中啤酒冒出大量气泡
B.对反应2NO2(g)![]() N2O4(g), 压缩体积平衡体系颜色变深
N2O4(g), 压缩体积平衡体系颜色变深
C.对SO2催化氧化成SO3的反应,往往加入过量的空气提高SO2转化率
(3)在一定条件下,将H2和N2置于容积为2 L的密闭容器中发生N2(g) + 3H2(g) ![]() 2NH3(g)反应,若充入N2(g)为0.80 mol和H2(g)为1.60 mol,反应在一定条件下达到平衡时,NH3的体积分数为20%,计算出相同温度下反应2NH3(g)
2NH3(g)反应,若充入N2(g)为0.80 mol和H2(g)为1.60 mol,反应在一定条件下达到平衡时,NH3的体积分数为20%,计算出相同温度下反应2NH3(g)![]() N2(g) + 3H2(g)的平衡常数为____________;
N2(g) + 3H2(g)的平衡常数为____________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com