
| A�����ȷ�Ӧ�У��»�ѧ���γ��������������ȷ�Ӧ�У��»�ѧ���γɷų����� |
| B��������������������Ƿֱ���ȫȼ�գ����߷ų��������� |
| C����ͬ���Ũ�Ⱦ�Ϊ0.1mol/L����ʹ�����Һ�ֱ���������NaOHϡ��Һ��Ӧ��ǰ�߷ų������� |
| D��������ȼ����Ϊ285.8kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8kJ/mol |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
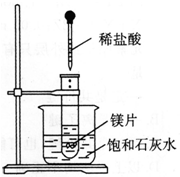
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȷ�Ӧ�ķ������������ |
| B�����Ⱥ���ܷ����ķ�Ӧ�������ȷ�Ӧ |
| C�����ʷ�����ѧ��Ӧ�������������仯 |
| D�����������仯�����ʱ仯���ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��485.5kJ/mol | B��610kJ/mol |
| C��917kJ/mol | D��1220kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A����Ӧ�Ļ�ѧ����ʽΪ5Y?X |
| B��t1ʱ��Y��Ũ����XŨ�ȵ�1.5�� |
| C��t2ʱ�������淴Ӧ������� |
| D��t3ʱ���淴Ӧ���ʴ�������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��0��3 min��X��ƽ����Ӧ����v(X)��0.2 mol��L��1��min��1 |
B��������Ӧ�ķ���ʽ�ɱ�ʾΪ��3X(g)��Y(g)  2Z(g) 2Z(g) |
| C�����������������䣬����ѹǿ��ƽ��������Ӧ�����ƶ� |
| D���¶Ȳ��䣬����X��Ũ�ȣ��÷�Ӧ��ƽ�ⳣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2G(g)���й��������£�
2G(g)���й��������£�| | E��g�� | F��g�� | G��g�� |
| ��ʼŨ�ȣ�mol?L-1�� | 2.0 | 1.0 | 0 |
| ƽ��Ũ�ȣ�mol?L-1�� | c1 | c2 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2Fe3++S2-====2Fe2++S�� | B��Fe3++H2S====Fe2++S��+2H+ |
| C��2Fe3++H2S====Fe2++S��+2H+ | D��2FeCl3+S2-====2FeCl2+S��+2Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com