
| A. | 因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 | |
| B. | 在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀 | |
| C. | 11.2 g Fe在高温下与足量水蒸气反应,生成的H2分子数目为0.3×6.02×1023 | |
| D. | 室温下,体积、pH均相同的HA和HB两种酸分别与足量的锌反应,HA放出的氢气多,说明酸性HB>HA |
分析 A.根据不同合金的材料和性能解答;
B.先达到离子积的先沉淀;
C.Fe在高温下与足量水蒸气反应生成四氧化三铁和氢气,3mol铁生成4mol氢气;
D.等体积pH均相同HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大.
解答 解:A.不是所有的合金耐腐蚀都很差,例如钛合金、铝合金等具有很好的抗腐蚀性能,故A错误;
B.先达到离子积的先沉淀,可能先生成白色沉淀,故B错误;
C.Fe在高温下与足量水蒸气反应生成四氧化三铁和氢气,3mol铁生成4mol氢气,故11.2 g Fe在高温下与足量水蒸气反应,生成的H2分子数目为$\frac{11.2}{56}$×$\frac{4}{3}$×6.02×1023=$\frac{0.8}{3}$×6.02×1023,故C错误;
D.等体积pH=3的HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大,HA为弱酸,所以酸性HB>HA,故D正确.
故选D.
点评 本题考查了金属的腐蚀与防护,沉淀的生成,转移电子数的计算以及酸的电离,考查学生对基本知识的掌握程度,题目简单,属于基础题.


科目:高中化学 来源: 题型:选择题
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 50mL18mol•L-1浓硫酸与足量铜供热,转移电子数为0.9NA | |
| C. | 0.1molCl2通入含0.1molFeBr2溶液中,被氧化的溴离子数为0.2NA | |
| D. | 标准状况下,2.24LNO和足量O2反应生成物中含有NO2分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱石灰具有吸水性,可用于干燥氯气 | |
| B. | 甲醛能使蛋白质变性,可以用于食品防腐剂 | |
| C. | 炭具有强还原性,常用于冶炼钠、钾等金属 | |
| D. | 碳酸氢钠溶液具有弱碱性,可用于制胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
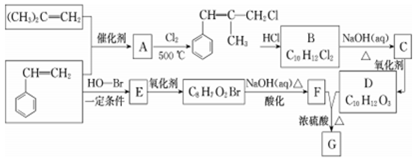
 .G的结构简式为
.G的结构简式为 .
.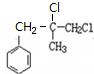 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$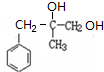 +2NaCl.
+2NaCl.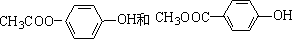 .
.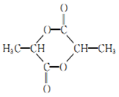 的合成路线:
的合成路线: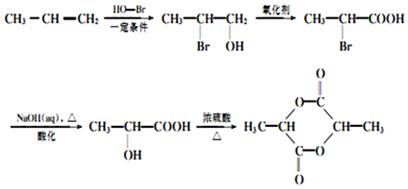 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
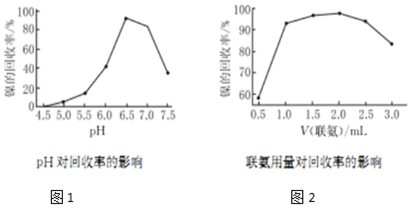
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 含有大量Fe3+的溶液中:Na+、Fe2+、Br-、SO42- | |
| B. | 1.0 mol/L KMnO4的溶液中:H+、Na+、Cl-、SO42- | |
| C. | 能与铝反应放出H2的溶液中:K+、Mg2+、SO42-、NO3- | |
| D. | 水电离的c(H+)和C(OH-)之积为l×l0-20mol2•L-2的溶液中:Na+、K+、CO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
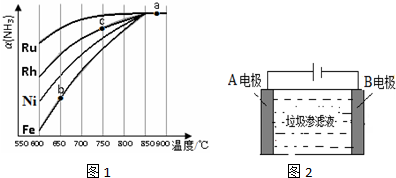
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
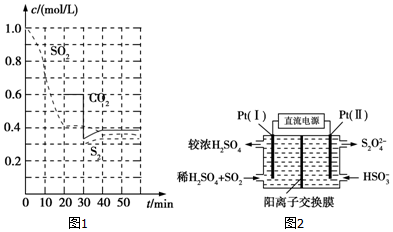
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com