
 某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:
某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
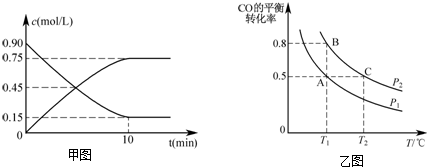
分析 (1)T1℃时,20min处于平衡状态,平衡时B、D、E的物质的量分别为1mol、0.5mol、0.5mol,反应气体气体体积不变,用物质的量代替浓度代入平衡常数表达式K=$\frac{c(D)×c(E)}{{c}^{2}(B)}$计算;
(2)30min改变改变,40min又到达平衡,B增大0.2mol,D、E分别增大0.1mol,平衡正向移动,可能是增大B的物质的量,由平衡常数可知各组分物质的量变化相同倍数也可以;
(3)与原平衡为完全等效平衡,按化学计量数转化到之比满足n(B)=2mol,由于原平衡中消耗的A为0.5mol,且A的为固体,A的用量增大不影响平衡移动,故按化学计量数转化到之比满足n(A)≥0.5mol;
(4)反应正向进行,表示出平衡时各组分物质的量,再根据平衡常数列方程计算解答;
(5)B的转化率最大时到达平衡,之前未到达平衡,随温度升高转化率增大,平衡后升高温度,B的转化率降低,说明升高温度平衡逆向移动,正反应为放热反应.
解答 解:(1)T1℃时,20min处于平衡状态,平衡时B、D、E的物质的量分别为1mol、0.5mol、0.5mol,反应气体气体体积不变,可以用物质的量代替浓度计算平衡常数,则K=$\frac{c(D)×c(E)}{{c}^{2}(B)}$=$\frac{0.5×0.5}{{1}^{2}}$=0.25,
故答案为:0.25;
(2)30min改变改变,40min又到达平衡,B增大0.2mol,D、E分别增大0.1mol,平衡正向移动,可能是增大B的物质的量,由平衡常数可知各组分物质的量变化相同倍数也可以,同时加入0.2molB、0.1molD、0.1molE也可以,
故选:ad;
(3)与原平衡为完全等效平衡,按化学计量数转化到之比满足n(B)=2mol,由于原平衡中消耗的A为0.5mol,且A的为固体,A的用量增大不影响平衡移动,故按化学计量数转化到之比满足n(A)≥0.5mol,所以生成D、E的量为0.5-0.2=0.3mol,A的量要够转化所以A的量不小于0.3mol,
故答案为:0.3;
(4)反应正向进行,生成0.5molE,则:
A(s)+2B(g)?D(g)+E(g)
起始量(mol):3 a 0
变化量(mol):1 0.5 0.5
平衡量(mol):2 a+0.50 0.50
所以$\frac{0.5×(a+0.5)}{{2}^{2}}$=0.25,解得a=1.5,
故答案为:1.5;
(5)B的转化率最大时到达平衡,则c点v(正)=v(逆),之前未到达平衡,随温度升高转化率增大,平衡后升高温度,B的转化率降低,说明升高温度平衡逆向移动,正反应为放热反应,则Q<0,
故答案为:<;=.
点评 本题考查化学平衡计算与影响因素、平衡常数及其应用等,(3)为易错点,由于A为固体不影响平衡移动,学生认为A的用量无关,忽略A的用量应保证可以转化得到D、E的量.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-542.7 kJ•mol-1 | |
| B. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1 059.3 kJ•mol-1 | |
| C. | N2H4(g)+$\frac{1}{2}$N2O4(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-1 076.7 kJ•mol-1 | |
| D. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1 076.7 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑ | |
| B. | Fe3O4与过量的稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向Ba(OH)2 溶液中逐滴加入NaHSO4溶液至溶液恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | Na2S溶液呈碱性:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Cl2、漂白液在生产、生活中广泛用于杀菌、消毒.回答下列问题:
Cl2、漂白液在生产、生活中广泛用于杀菌、消毒.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( )
X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( ) | A. | ①② | B. | ③④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com