
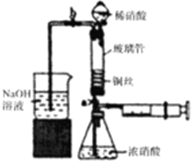
 利用下列装置可实现铜与浓硝酸、稀硝酸反应,过程如下:
利用下列装置可实现铜与浓硝酸、稀硝酸反应,过程如下:| 实验编号 | 水温/℃ | 液面上升高度 |
| 1 | 25 | $\frac{2}{3}$ |
| 2 | 50 | 不足试管的$\frac{2}{3}$ |
| 3 | 0 | 液面上升超过实验1 |
分析 (1)铜绿的主要成分为Cu2(OH)2CO3,铜在空气中与水、二氧化碳和氧气生成铜绿;
(2)将铜丝烧成螺旋状可增大反应的表面积,结合压强差原理检查气密性;
(3)①浓硝酸与铜丝接触反应生成红棕色二氧化氮气体;反应停止的操作是铜和浓硝酸分离;
②稀硝酸充满玻璃管的实验目是将玻璃管中的NO2和空气排出,铜和稀硝酸反应生成硝酸铜一氧化氮和水;
(4)①依据图表数据分析温度越低进入液体越多;
②NO2与水反应:3NO2+H2O=2HNO3+NO,如NO2完全反应,则生成NO$\frac{V}{3}$L,进入水的体积为$\frac{2V}{3}$L,如通入氧气,则发生4NO2+O2+H2O=4HNO3,结合反应计算.
解答 解:(1)铜绿的主要成分为Cu2(OH)2CO3,铜在空气中与水、二氧化碳和氧气生成铜绿,反应的方程式为2Cu+CO2+O2+H2O=Cu2(OH)2CO3,
故答案为:2Cu+CO2+O2+H2O=Cu2(OH)2CO3;
(2)将铜丝烧成螺旋状可增大反应的表面积,增大反应速率;气密性检查是依据装置中的气体压强变化和液面变化,打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好,
故答案为:增大铜丝与酸的接触面积,提高化学反应速率;打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好;
(3))①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触反应生成红棕色二氧化氮气体;一段时间后使反应停止的操作是轻轻将注射器活塞向右拉使铜丝和溶液分开,
故答案为:产生红棕色气体;轻轻将注射器活塞向右拉使铜丝和溶液分开;
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是将玻璃管中的NO2和空气排出;稀硝酸和铜反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
故答案为:将玻璃管中的NO2和空气排出;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)①温度越低,液体进入试管的越多,故答案为:低;
②NO2与水反应:3NO2+H2O=2HNO3+NO,如NO2完全反应,则生成NO$\frac{V}{3}$L,进入水的体积为$\frac{2V}{3}$L,生成硝酸的物质的量为$\frac{\frac{2V}{3×22.4}mol}{\frac{2V}{3}L}$=$\frac{1}{22.4}$mol/L,
如通入氧气,则发生4NO2+O2+H2O=4HNO3,如NO2完全反应,则应该充入氧气的体积是$\frac{V}{4}$L,
故答案为:$\frac{1}{22.4}$;$\frac{V}{4}$L.
点评 本题考查性质实验的设计,侧重于硝酸性质的分析应用,为高频考点,答题时注意把握装置图的结构和反应原理,掌握物质性质和反应现象是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | R元素处于第三周期ⅥA族 | B. | R元素是较活泼的非金属元素 | ||
| C. | 原子核外共有14个电子 | D. | 元素最低化合价为-2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数为2的元素一定处于周期表IIA族 | |
| B. | 主族元素X、Y能形成XY2型化合物,则X与Y 的原子序数之差可能为2或5 | |
| C. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| D. | 同主族元素形成的氧化物的晶体类型均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3+CO32- | |
| B. | 硫酸酸化的淀粉KI溶液在空气中变成蓝色:4I++O2+2H2O═2I2+4OH- | |
| C. | 钢铁发生吸氧腐蚀时,正极的电极反应式:O2+4e-+2H2O═4OH- | |
| D. | 氨气催化氧化生产硝酸的主要反应:4NH3+7O2$\frac{\underline{\;催化剂\;}}{高温}$4NO2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、NO3-、Cl-、 | B. | H+、Fe2+、ClO-、SO42- | ||
| C. | K+、Fe3+、C6H5O-、SCN- | D. | NH4+、Al3+、SiO32-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100℃时,KW=10-12,此温度下pH=6的溶液一定显酸性 | |
| B. | 25℃时,0.1mol/L的NaHSO3溶液pH=4,说明该溶液中c(HSO3-)>c(SO32-) | |
| C. | NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | |
| D. | 25℃时,10mL0.1mol/L CH3COOH溶液与5mL 0.1mol/LNaOH溶液混合,所得溶液中有2c(Na+)═c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| B. | 标准状况下,11.2 L CCl4中含有的分子数目为0.5NA | |
| C. | 28 g聚乙烯中含有的碳原子数目为2NA | |
| D. | 1 mol C${{H}_{5}}^{+}$中含有的电子数目为11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 1 L 1mol/L的盐酸含有NA个HCl分子 | |
| C. | 标准状况下,33.6 L四氯化碳中含有氯原子的数目为6NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com