
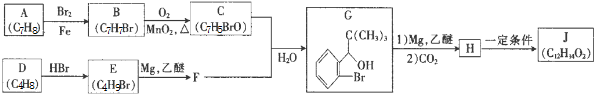
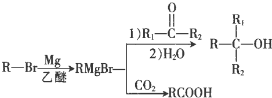
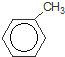
 +Br2$\stackrel{铁粉}{→}$
+Br2$\stackrel{铁粉}{→}$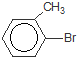 +HBr.,其反应类型为取代反应;
+HBr.,其反应类型为取代反应;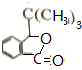 ,由D生成E的化学反应方程式为CH2=C(CH3)2+HBr→(CH3)3CBr;
,由D生成E的化学反应方程式为CH2=C(CH3)2+HBr→(CH3)3CBr;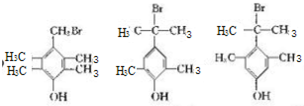 (其中一种)(写出一种即可).
(其中一种)(写出一种即可). 分析 比较A、B的分子式可知,A与HBr发生加成反应生成B,B的核磁共振氢谱只有一组峰,则可知D为CH2=C(CH3)2,E为(CH3)3CBr,根据题中已知①可知F为(CH3)3CMgBr,C能发生银镜反应,同时结合G和F的结构简式可推知C为 ,进而可以反推得,B为
,进而可以反推得,B为 ,A为
,A为 ,根据题中已知①,由G可推知H为
,根据题中已知①,由G可推知H为 ,J是一种酯,分子中除苯环外,还含有一个五元环,则J为
,J是一种酯,分子中除苯环外,还含有一个五元环,则J为 ,
, 与溴发生取代生成K为
与溴发生取代生成K为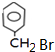 ,K在镁、乙醚的条件下生成L为
,K在镁、乙醚的条件下生成L为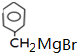 ,L与甲醛反应生成2-苯基乙醇,据此答题.
,L与甲醛反应生成2-苯基乙醇,据此答题.
解答 解:比较A、B的分子式可知,A与HBr发生加成反应生成B,B的核磁共振氢谱只有一组峰,则可知D为CH2=C(CH3)2,E为(CH3)3CBr,根据题中已知①可知F为(CH3)3CMgBr,C能发生银镜反应,同时结合G和F的结构简式可推知C为 ,进而可以反推得,B为
,进而可以反推得,B为 ,A为
,A为 ,根据题中已知①,由G可推知H为
,根据题中已知①,由G可推知H为 ,J是一种酯,分子中除苯环外,还含有一个五元环,则J为
,J是一种酯,分子中除苯环外,还含有一个五元环,则J为 ,
, 与溴发生取代生成K为
与溴发生取代生成K为 ,K在镁、乙醚的条件下生成L为
,K在镁、乙醚的条件下生成L为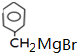 ,L与甲醛反应生成2-苯基乙醇,
,L与甲醛反应生成2-苯基乙醇,
(1)由A生成B的化学方程式为 +Br2$\stackrel{铁粉}{→}$
+Br2$\stackrel{铁粉}{→}$ +HBr,其反应类型为取代反应,
+HBr,其反应类型为取代反应,
故答案为: +Br2$\stackrel{铁粉}{→}$
+Br2$\stackrel{铁粉}{→}$ +HBr;取代反应;
+HBr;取代反应;
(2)D为CH2=C(CH3)2,名称是2-甲基丙烯,故答案为:2-甲基丙烯;
(3)根据上面的分析可知,J的结构简式为 ,由D生成E的化学方程式为CH2=C(CH3)2+HBr→(CH3)3CBr,
,由D生成E的化学方程式为CH2=C(CH3)2+HBr→(CH3)3CBr,
故答案为: ; CH2=C(CH3)2+HBr→(CH3)3CBr;
; CH2=C(CH3)2+HBr→(CH3)3CBr;
(4)G的同分异构体中核磁共振氢谱有4组峰且能与FeCl3溶液发生显色反应,说明有酚羟基,这样的结构为苯环上连有-OH、-CH2Br呈对位连结,另外还有四个-CH3基团,呈对称分布,或者是-OH、-C(CH3)2Br呈对位连结,另外还有2个-CH3基团,以-OH为对称轴对称分布,这样有 ,
,
故答案为: (其中一种).
(其中一种).
点评 本题考查有机物的推断,侧重于有机物官能团的性质以及学生分析能力的考查,解答本题的突破口为E的推断,答题时注意把握题给信息,体会做题思路,可采用逆推的方法推断,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
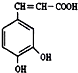 如图咖啡酸,存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
如图咖啡酸,存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.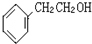 .
. 的一种同分异构体,A的苯环上有三个取代基,能发生银镜反应,苯环上的一氯代物有两种.写出A的一种结构简式:
的一种同分异构体,A的苯环上有三个取代基,能发生银镜反应,苯环上的一氯代物有两种.写出A的一种结构简式: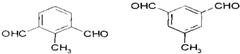 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠块沉在乙醇液面下面 | B. | 钠块熔成小球 | ||
| C. | 钠块在乙醇液面上游动 | D. | 钠块表面无气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6 kJ/mol
(1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6 kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题
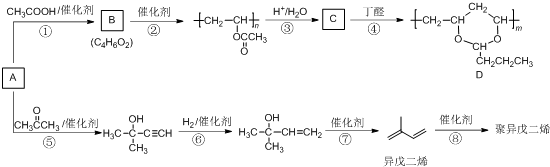
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3═2Na++CO32- | B. | H2O═2H++O2- | ||
| C. | HNO3═H++NO3- | D. | K2SO4═2K++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
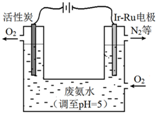 过氧化氢(H2O2)是淡蓝色的黏稠液体,水溶液为无色透明液体,俗称双氧水,可以看作二元弱酸.
过氧化氢(H2O2)是淡蓝色的黏稠液体,水溶液为无色透明液体,俗称双氧水,可以看作二元弱酸.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com