
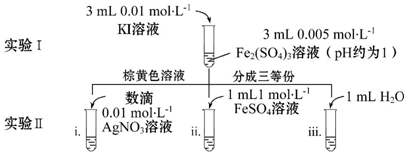
分析 (1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到化学平衡状态;
(2)加入AgNO3,Ag+与I-生成AgI黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动;
(3)加水向离子浓度变大的方向移动;加水的同时离子的浓度变小,所以ⅲ为实验ⅱ做参照对比;
(4)如实验Ⅱ中,ⅱ的现象溶液颜色变得比ⅲ更浅,即能证明增大生成物浓度化学平衡发生了逆向移动;
(5)正反应是放热反应,可以通过改变温度使平衡移动,也可以增加碘单质的浓度,使平衡移动.
解答 解:(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到化学平衡状态,否则干扰平衡移动的判断,故答案为:化学平衡状态; (1)反应达平衡状态
(2)加入AgNO3,Ag+与I-生成AgI黄色沉淀,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动,可知Fe2+向Fe3+转化,故答案为:Ag+与I-生成AgI黄色沉淀,溶液颜色变浅,I-浓度降低,2Fe3++2I-?2Fe2++I2平衡逆向移动,溶液颜色变浅;
(3)加水向离子浓度变大的方向移动,所以反应逆向移动;加水的同时离子的浓度变小,所以不能说明因平衡移动导致离子浓度减小,所以ⅲ为实验ⅱ做参照对比,故答案为:逆反应方向;不能;为实验ⅱ做参照;
(4)如实验Ⅱ中,ⅱ的现象溶液颜色变得比ⅲ更浅,即能证明增大生成物浓度化学平衡发生了逆向移动,故答案为:溶液颜色变得比ⅲ更浅;
(5)正反应是放热反应,可以通过升高温度使平衡逆向向移动,也可以增加碘单质的浓度,使平衡逆向移动,故答案为:加热(加入浓碘水).
点评 本题考查化学平衡移动的综合考查,把握平衡移动的影响因素及物质的性质为解答的关键,对分析与实验能力要求较高,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 硫化氢气体通入硫酸铜溶液中:S2-+Cu2+=CuS↓ | |
| B. | 4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+ | |
| C. | Ba(OH)2溶液中加入少量的NaHSO4溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| D. | NaHCO3的水解:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠的化学式:NaCl2 | |
| B. | 镁的原子结构示意图: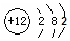 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 碳酸钠的电离方程式:Na2CO3=Na++CO32一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入FeCl3固体 | B. | 加水 | C. | 加入少量浓盐酸 | D. | 升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L H2O含有NA个分子 | |
| B. | 0.1 mol Cl2与足量NaOH溶液反应,转移电子数为0.2 NA | |
| C. | 0.1 mol AlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子 | |
| D. | 1L 1 mol•L-1的NaClO 溶液中含有ClO-的数目少于NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,NA个SO3的体积为22.4 L | |
| B. | 1 mol Fe与足量的HCl溶液反应,转移的电子数为3NA | |
| C. | 2 L 1 mol•L-1的H3PO4溶液中所含的H+数为6NA | |
| D. | 标准状况下22.4 L Cl2通入足量的石灰乳制备漂白粉,转移电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com