
| V(NaOH) | V(KHP)平均 |
| 20.00mL | 18.00mL |
| V(稀释后的醋) | V(NaOH)平均 |
| 18.00mL | 20.00mL |
| ||
| 0.1L |
| ||
| 0.1L |
| 0.01L×0.6mol/L |
| 0.1mol/L |
| 0.101mol/L×0.018L |
| 0.018L |
| 0.101 |
| 0.1 |


科目:高中化学 来源: 题型:
| A、利用化学平衡常数判断化学反应进行的快慢 |
| B、利用溶解度数据判断氧化还原反应发生的可能性 |
| C、利用沸点数据推测将一些液体混合物分离的可能性 |
| D、利用物质的摩尔质量判断相同状态下不同物质密度的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
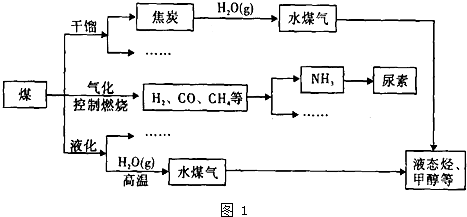
| 化学键 | C-H | H-O | H-H | C-O | C=O |
| 键能/KJ mol-1 | 413 | 463 | 436 | 358 | 802 |
 CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是
CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是| CH3OH(g) | CH3OCH3(g) | H2O(g) | |
| 起始浓度/mol?L-1 | 2.00 | 0.50 | 0 |
| 平衡浓度/mol?L-1 | c1 | 1.00 | c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
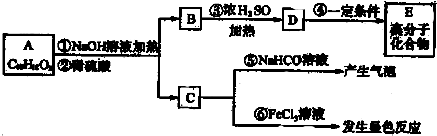
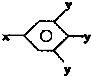 (其中-x、一y均为官能团).请回答下列问题:
(其中-x、一y均为官能团).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
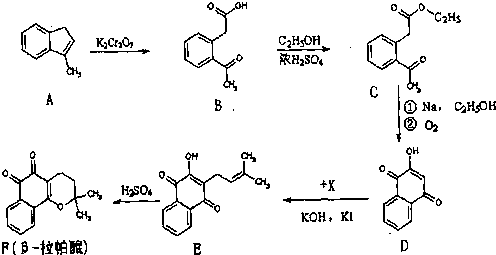
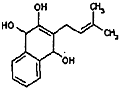 ,写出此有机物分子中含有的官能团名称:
,写出此有机物分子中含有的官能团名称: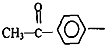 结构且能水解的所有同分异构体的结构简式:
结构且能水解的所有同分异构体的结构简式:查看答案和解析>>
科目:高中化学 来源: 题型:
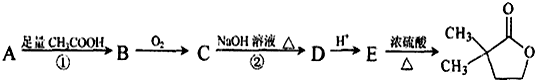
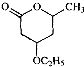 是B的一种重要的同分异构体.请设计合理方案,完成从
是B的一种重要的同分异构体.请设计合理方案,完成从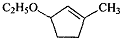 到
到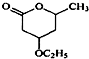 的合成路线(用流程图表示,并注明反应条件).
的合成路线(用流程图表示,并注明反应条件).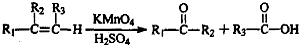 ;
;| 浓硫酸 |
| 170℃ |
| 高温、高压 |
| 催化剂 |
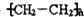 .
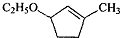
.
| H2O |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用醋酸溶液除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
| B、向FeBr2溶液中通入足量Cl2:Fe3++2Br-+Cl2═Fe3++Br2+2Cl- |
| C、向Na[Al(OH)4]溶液中通入过量CO2:[Al(OH)4]-+CO2═Al(OH)3↓+HCO3- |
| D、向Ba(OH)2溶液滴加NaHSO4溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制作航天服的聚酯纤维和用于制光缆的光导纤维都是新型无机非金属材料 |
| B、使用太阳能、风能等清洁能源能减少PM2.5的污染 |
| C、水泥、玻璃、水晶饰物都是硅酸盐制品 |
| D、用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com