
����Ŀ������ͼ�а�������Ϣ����������������ȷ���ǣ� ��

A��������������Ӧ����1mol�Ȼ������壬��Ӧ����248kJ������
B��436kJ/mol��ָ�Ͽ�1molH 2 �е�H-H����Ҫ�ų�436kJ������
C��431kJ/mol��ָ����2molHCl�е�H-Cl����Ҫ�ų�431kJ������
D��������������Ӧ����2mol�Ȼ������壬��Ӧ�ų�183kJ������
���𰸡�D
��������
���������A����Ӧ����2mol�Ȼ�������ų���������431kJ/mol��2mol-436kJ/mol-238kJ/mol=183kJ/mol����A���� B��436kJ/mol��ָ�Ͽ�1molH2�е�H-H����Ҫ����436kJ����������B����C��431kJ/mol��ָ����1molHCl�е�H-Cl����Ҫ�ų�431kJ����������C����D����Ӧ����2mol�Ȼ�������ų���������431kJ/mol��2mol-436kJ/mol-243kJ/mol=183kJ/mol����D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2014��پ�)A��B��D��E��FΪ������Ԫ�أ��ǽ���Ԫ��A����������������������ͬ��B����������������������������2����B ��D�г��ȼ������������ۻ�����BD2��E����D2��������ͬ�ĵ�������A��F��ȼ�գ���������ˮ�õ�һ��ǿ�ᡣ�ش�����������
��1��A�����ڱ��е�λ���� ��д��һ�ֹ�ҵ�Ʊ�����F�����ӷ���ʽ ��
��2��B��D��E��ɵ�һ�����У�E����������Ϊ43%��������Ϊ ����ˮ��Һ��F���ʷ�Ӧ�Ļ�ѧ����ʽΪ ���ڲ����м�����
��KI����Ӧ�����CC14������ ������ ɫ��
��3������ЩԪ����ɵ����ʣ�����ɺͽṹ��Ϣ���±���
���� | ��ɺͽṹ��Ϣ |
a | ����A�Ķ�Ԫ���ӻ����� |
b | ���зǼ��Թ��ۼ��Ķ�Ԫ���ӻ������ԭ����֮��Ϊ1:1 |
c | ��ѧ���ΪBDF2 |
d | ֻ����һ�������������ҿɵ���ĵ��ʾ��� |
a�Ļ�ѧʽΪ ��b�Ļ�ѧʽΪ ����c�ĵ���ʽΪ ��
d�ľ��������� ��
��4����A��B��DԪ����ɵ����ֶ�Ԫ�������γ�һ������Դ���ʡ�һ�ֻ��������ͨ�� ����
�ɾ��п�ǻ�Ĺ�������һ�ֻ�����(��������Ҫ�ɷ�)���ӽ���ÿ�ǻ������ӵĿռ�ṹΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ�����������ȷ���ǣ� ��
A. ��Ũ��ˮϴ������������Ӧ���Թ�
B. �÷�Һ©�����뻷�����ˮ�Ļ��Һ��
C. ����ʯ��ʱ���¶ȼƵ�ĩ�˱������Һ����
D. ��������Cu��OH��2��Һʱ����2mL10% CuSO4��Һ�е��뼸��2%NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������£���������ķ�����һ����ȵ���
A��ͬ�ܶȡ�ͬѹǿ�� N2 �� C2H4 B��ͬ�����ͬ�ܶȵ�C2H4��CO
C��ͬ�¶ȡ�ͬ����� O2��N2 D��ͬѹǿ��ͬ����� O2�� N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A����֪C2H6��ȼ����Ϊ1090 kJ��mol��1������ʾC2H6ȼ�������Ȼ�ѧ����ʽΪ��
C2H6��g����![]() O2��g�� = 2CO2��g����3H2O��g�� ��H����1090 kJ��mol��1
O2��g�� = 2CO2��g����3H2O��g�� ��H����1090 kJ��mol��1
B����֪2CO��g����O2��g�� = 2CO2��g�� ��H����566 kJ��mol��1����CO��ȼ���Ȧ�H����283 kJ
C���ⶨHCl��NaOH��Ӧ���к���ʱ��ÿ��ʵ���Ӧ����3���¶�
D����ϡ��Һ�У�H+��aq��+OH-��aq��=H2O��l�� ��H=��57.3kJ��mol��1��˵��ϡ������ϡNaOH��Һ��Ӧ����1 mol H2O��l��ʱ�ų�57.3 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a1��a2�ֱ�ΪA�ڼס����������������н���ƽ����ϵA(g)![]() 2B(g)ʱ��ת���ʣ���֪����������ѹǿ���䣬��������������������䡣���¶Ȳ��������£�������A�����ʵ����������ж���ȷ����( )
2B(g)ʱ��ת���ʣ���֪����������ѹǿ���䣬��������������������䡣���¶Ȳ��������£�������A�����ʵ����������ж���ȷ����( )
A��a1��a2����С B��a1��С��a2����
C��a1�����䣬a2���� D��a1���䣬a2��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϣ�����ࡢ��Ч�����������Ļ������ܣ�������һ����ɫ���壬������������ζ����ȼ����Ϊ1455 kJ��mol��1�����ѿ���ȼ�ϵ�ص�ȼ�ϣ�
��1��д������ȼ�յ��Ȼ�ѧ����ʽ ����֪H2��g����C��s����ȼ���ȷֱ���285.8kJ��mol��1��393.5kJ��mol��1�����㷴Ӧ4C��s��+6H2��g��+O2��g���T2CH3OCH3��g���ķ�Ӧ����H= kJ��mol��1��
��2����ҵ������H2��CO2�ϳɶ����ѵķ�Ӧ���£�6H2��g��+2CO2��g��![]() CH3OCH3��g��+3H2O��g����H��0
CH3OCH3��g��+3H2O��g����H��0
��һ���¶��£���һ���̶�������ܱ������н��и÷�Ӧ���������жϷ�Ӧ�ﵽ��ѧƽ��״̬���� ��ѡ���ţ�ע���Сд����
a��c��H2����c��H2O���ı�ֵ���ֲ���
b����λʱ������2mol H2����ʱ����1mol H2O����
c�������������ܶȲ��ٸı�
d������������ѹǿ���ٸı�
���¶����ߣ��û�ѧƽ���ƶ��ﵽ�µ�ƽ�⣬CH3OCH3�IJ��ʽ� ����������С�����䡱����ͬ����
��3���Լ��ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�أ��õ�صĸ�����Ӧʽ������һ��������CO32������д���÷�Ӧ�ĸ�����Ӧʽ ��
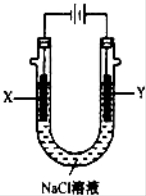
��4���ã�3���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500mL NaCl��Һ��װ����ͼ��ʾ����д����������Y�缫�����۲쵽�������� ����ȼ�ϵ������2.8LO2����״���£�ʱ�������ʱ��NaCl��Һ��C(OH-)= mol/L��������Һ��������䣬����ȫ������Һ���ݳ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǽ�������ǿ��Ԫ����Ԫ�����ڱ��ģ� ��
A.���Ϸ�
B.���·�
C.���·�
D.���Ϸ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ã���ɺܶ�绯ѧʵ�飮�����йش�װ�õ������У���ȷ����

A����XΪп����YΪNaCl��Һ������K����M�����ɼ������ĸ�ʴ�����ַ�����Ϊ��������������
B����XΪ̼����YΪNaCl��Һ������K����N�����ɼӿ����ĸ�ʴ
C����XΪͭ����YΪ����ͭ��Һ������K����M����ͭ�����������ӣ���ʱ���·�еĵ�����ͭ�缫�ƶ�
D����XΪͭ����YΪ����ͭ��Һ������K����N�����������������ͭ����Һ��ͭ����Ũ�Ƚ���С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com