
【题目】由分别与氖和氩电子层结构相同的两种离子组成的化合物是( )
A. MgF2 B. SO2 C. Na2O D. Na2S
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠晶体(Na2S2O3·5H2O)俗名海波,又名“大苏打”,是无色单斜晶体。易溶于水,不溶于乙醇,具有较强的还原性,广泛地应用于照相等工业中。回答下列问题:
(1)Na2S2O3·5H2O属于______(填“纯净物”或“混合物”)。
(2)酸性条件下,S2O32-自身发生氧化还原反应生成SO2。试写出Na2S2O3与盐酸反应的离子方程式:_____。
(3)亚硫酸法制备Na2S2O3·5H2O简易流程如下:
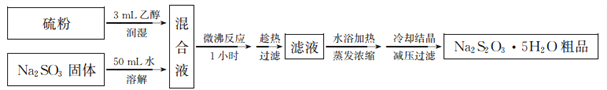
①Na2S2O3·5H2O制备原理为_________________(用化学方程式表示)。
②Na2S2O3·5H2O粗品中可能含有Na2SO3、Na2SO4杂质,其检验步骤为:取适量产品配成稀溶液,滴加足量氯化钡溶液,有白色沉淀生成;将白色沉淀过滤,先用蒸馏水洗涤沉淀,然后向沉淀中加入足量____(填试剂名称),若_______________(填现象),则证明产品中含有Na2SO3和Na2SO4(已知:Na2S2O3稀溶液与BaCl2溶液无沉淀生成)。
③粗品中Na2S2O3·5H2O的质量分数的测定
称取6g粗品配制250 ml.的溶液待用。另取25 ml.0.01 mol/L K2Cr2O7溶液于锥形瓶中,然后加入过量的KI溶液并酸化和几滴淀粉溶液,立即用配制的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25mL。粗品中Na2S2O3·5H2O的质量分数为________。已知Cr2O72-+6I-+ 14 H+ =2Cr3++ 3I2+7H2O、I2+2S2O32- =2I-+S4O62-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖在不同条件下可以被氧化成不同物质。请结合题意回答问题:已知:RCOOH+CH2===CH2+![]() O2
O2![]() RCOOCH===CH2+H2O
RCOOCH===CH2+H2O
(1)葡萄糖在酒化酶作用下生成有机物A,A、B、C、D、E间的转化关系如下图所示:

①B是石油化学工业最重要的基础原料,写出A→B的化学方程式:___________________________________________。
②D的结构简式为_____________________________。
(2)葡萄糖在一定条件下还可氧化为X和Y(Y和A的相对分子质量相同)。X可催化氧化成Y,也可与H2反应生成Z。X和Y的结构中有一种相同的官能团是________,检验此官能团需用的试剂是________。
(3)F是人体肌肉细胞中的葡萄糖在缺氧的条件下进行无氧呼吸的产物。F、G、H间的转化关系是:F![]() G
G![]() H,H与(1)中的D互为同分异构体。
H,H与(1)中的D互为同分异构体。
①G还可以发生的反应有________(填字母)
a.加成反应 b.水解反应 c.氧化反应 d.消去反应 e.还原反应
②本题涉及的所有有机物中,与F不论以何种质量比混合(总质量一定),完全燃烧生成CO2和H2O的物质的量不变的有(写结构简式)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸铁铵[(NH4)3Fe( C6 H5O7)2,摩尔质量488 g/mol] 是一种重要的食品添加剂。一种制备柠檬酸铁铵的实验步骤如下:

步骤1.在右图三颈烧瓶中加入16.7 g FeSO4·7H2O、40 ml.蒸馏水,3mL硫酸和1 g NaClO3,强力搅拌;
步骤2.升温至80℃,再补加l g NaClO3;
步骤3.向反应器中加入NaOH溶液,温度控制在80~90℃,剧烈搅拌;
步骤4.过滤,洗涤,沥干,得活性Fe(OH)3;
步骤5.将Fe(OH)3和一定量的水加入三颈烧瓶中,控制95℃以上,加入计算量的柠檬酸溶液,搅拌,并保温1h;
步骤6.冷却到50℃,搅拌下加入氨水40 mL,静置、浓缩至膏状,80℃干燥得柠檬酸铁铵24.9 g。
回答下列问题:
(1)步骤1发生反应的离子方程式为_____________________________。
(2)步骤2再补加NaClO3的目的是_____________________________。
(3)步骤3确定Fe3+已沉淀完全的方法是_____________________________。
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要_____________________________;证明Fe(OH)3已被洗涤干净的方法为__________________________。
(5)柠檬酸铁铵的产率为_________(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L 0.2 mol/L的KI溶液中,含溶质KI的物质的量是
A. 0.2 mol B. 0.5 mol C. 2 mol D. 5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极,已知:装置的电流效率等于生成产品所需的电子数与电路中通过总电子数之比。下列说法错误的是( )

A. 该装置中Y电极发生氧化反应
B. X电极的电极反应式为 6CO2+24H++24e-=== C6H12O6+6H2O
C. 理论上,每生成22.4 L(标准状况下)O2,必有4 mol H+由X极区向Y极区迁移
D. 当电路中通过3 mol e时,生成18 g C6H12O6,则该装置的电流效率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A. Ag+、K+、Cl-、NO3-
B. Ba2+、Cl-、H+、SO42-
C. H+、CO32-、Cl-、Na+
D. Na+、Ba2+、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列的物理量不再发生变化时,表明反应A(固)+2B(气)![]() C(气)+D(气)已达到平衡状态的是( )
C(气)+D(气)已达到平衡状态的是( )
A. 混合气体的压强 B. 混合气体的密度
C. 气体的总物质的量 D. A的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com