
| 时间(min) | n(A)(mol) | n(B)(mol) | n(C)(mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
分析 在前2min内,各物质的浓度的变化量之比(1-0.8):(3-2.6):(0.4-0)=1:2:2,则方程式为A (g)+2B(g)?2C(g),
(1)A物质的化学反应速率v(A)=$\frac{△c}{t}$,代入数据进行计算即可;
(2)影响化学反应速率的因素有:使用催化剂、改变温度、浓度、改变物质的表面积等;
(3)求出第4min时各物质的浓度,根据平衡常数计算公式计算即可;
(4)根据Qc=$\frac{c{\;}^{2}(C)}{c(A)•{c}^{2}(B)}$,计算第9min时Qc的值,与K比较;
解答 解:在前2min内,各物质的浓度的变化量之比(1-0.8):(3-2.6):(0.4-0)=1:2:2,则方程式为A (g)+2B(g)?2C(g),
(1)第2min到第4min内A物质的化学反应速率v(A)=$\frac{△c}{t}$=$\frac{\frac{(0.8-0.4)mol}{2L}}{2min}$=0.1mol/(l•min),
故答案为:0.1;
(2)①在第0~2min内,A的物质的量减小了0.2mol,在2~4min内A的物质的量在原基础上减小了0.4mol,化学反应速率加快了,可以是使用催化剂或升高温度,
故答案为:使用催化剂、升高温度;
②第6min 到第8min,作为反应物,浓度应该是减小的趋势,但是B的物质的量从1.8mol增加到了2.0mol,而A在减小,C在增大,所以可知一定是加入了B物质,
故答案为:增加B的浓度;
(3)反应在第4min建立平衡,c(A)=$\frac{0.4mol}{2L}$=0.2mol/L,c(B)=$\frac{1.8mol}{2L}$=0.9mol/L,c(C)=$\frac{1.2mol}{2L}$=0.6mol/L,
则K=$\frac{c{\;}^{2}(C)}{c(A)•{c}^{2}(B)}$=$\frac{0.{6}^{2}}{0.2×0.{9}^{2}}$=2.22;
故答案为:2.22;
(4)Qc=$\frac{c{\;}^{2}(C)}{c(A)•{c}^{2}(B)}$=$\frac{({\frac{0.3}{2})}^{2}}{(\frac{0.05}{2})•(\frac{1.9}{2})^{2}}$=0.997<K=2.22,则反应未达到平衡状态;
故答案为:否,因为Qc<K.
点评 本题主要考查了影响化学反应速率的因素和有关反应速率的计算、化学平衡常数的定义以及计算等,题目难度中等,题目综合性较强,熟练掌握基础知识是解决此类题是关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 石灰石.高岭石.石英和水晶的主要成份都是硅酸盐 | |
| B. | 浓硫酸具有吸水性.脱水性,还可以做氧化剂 | |
| C. | 过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+ | |
| D. | 硅是应用广泛的半导体材料,常温下易与氧气、氯气、硫酸等物质反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
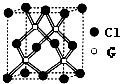 A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和.
A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和. ;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;
;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3可以做油漆的颜料 | B. | Al2O3可用作耐火材料 | ||
| C. | 王水可以雕刻玻璃 | D. | 赤铁矿可用作炼铁的原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用铂作催化剂 | B. | 降低温度 | ||
| C. | 缩小体积增大压强 | D. | 增大接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1mol•L-1 氯化钠溶液 | B. | 75mL 1mol•L-1 氯化钙溶液 | ||
| C. | 150mL 3mol•L-1 氯化钾溶液 | D. | 75mL 2mol•L-1 氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
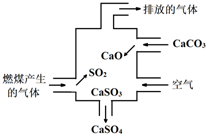
| A. | 使用此装置可减少导致酸雨的气体形成 | |
| B. | 用酸性高锰酸钾溶液检验废气处理是否达标 | |
| C. | 整个过程的总反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 | |
| D. | 排放的气体是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
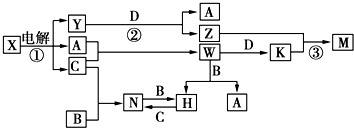
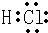 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com