
| ¼ÓĮņĖįµÄ“ĪŹżŠņŗÅ | ¼ÓČėĮņĖįµÄĢå»ż/mL | Ź£Óą¹ĢĢåµÄÖŹĮæ/g |
| 1 | 20.0 | 7.20 |
| 2 | 20.0 | 4.40 |
| 3 | 20.0 | 2.00 |
| 4 | 20.0 | 2.00 |
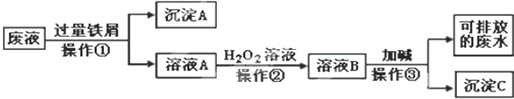
·ÖĪö £Ø1£©ĢśÓėĻ”ĮņĖį·“Ӧɜ³ÉĮņĖįŃĒĢśÓėĒāĘų£»
£Ø2£©·ÖĪö±ķÖŠŹż¾ŻæÉÖŖ£¬Ē°Į½“ĪĮņĖį¾ł²»×ć£¬ÓƵŚŅ»“ĪŹż¾Ż¼ĘĖć£¬µŚ1×éÖŠ²Ī¼Ó·“Ó¦µÄFeĪŖ10g-7.20g=2.80g£¬ĮņĖįĶźČ«·“Ó¦£¬øł¾Ż·½³ĢŹ½¼ĘĖć20mLČÜŅŗÖŠĮņĖįµÄĪļÖŹµÄĮ棬ŌŁøł¾Żc=$\frac{n}{V}$¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©ĢśÓėĻ”ĮņĖį·“Ӧɜ³ÉĮņĖįŃĒĢśÓėĒāĘų£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗFe+2H+=Fe2++H2”ü£¬
¹Ź“š°øĪŖ£ŗFe+2H+=Fe2++H2”ü£»
£Ø2£©±Č½Ļ±ķøńÖŠŹż¾ŻæÉŅŌ·¢ĻÖ£¬Ćæ¼ÓČė20mLĮņĖį£¬µŚ1”¢2“ĪŹ£Óą¹ĢĢåµÄÖŹĮæ¾ł¼õŠ”2.8gæĖ£¬¶ųµŚ3“Ī¼õÉŁ2.4g£¬¹ŹĒ°Į½“ĪĮņĖį¾ł²»×ć£¬ÓƵŚŅ»“ĪŹż¾Ż¼ĘĖć£¬µŚ1×éÖŠ²Ī¼Ó·“Ó¦µÄFeĪŖ£ŗ10g-7.20g=2.80g£¬
Fe+H2SO4=FeSO4+H2ӟ
56g 1mol
2.8g n
n=$\frac{2.8g”Į1mol}{56g}$=0.05mol
ŌņĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ£ŗ$\frac{0.05mol}{0.02L}$=2.5mol/L£¬
“š£ŗøĆĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ2.5mol/L£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·½³ĢŹ½µÄÓŠ¹Ų¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲæ¼²éѧɜ¶ŌŹµŃ鏿¾ŻµÄ·ÖĪö“¦ĄķÄÜĮ¦£¬øł¾Ż¹ĢĢåÖŹĮæ±ä»ÆÅŠ¶Ļ¹żĮæĪŹŹĒ½āĢā¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ»Æѧ¼ĘĖćÄÜĮ¦£®


 æŖŠÄĮ·Ļ°æĪæĪĮ·Óėµ„ŌŖ¼ģ²āĻµĮŠ“š°ø
æŖŠÄĮ·Ļ°æĪæĪĮ·Óėµ„ŌŖ¼ģ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į× | B£® | Ńõ | C£® | Ģś | D£® | äå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
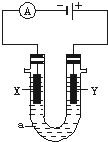 µē½āŌĄķŌŚ»Æѧ¹¤ŅµÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®ČēĶ¼±ķŹ¾Ņ»øöµē½ā³Ų£¬×°ÓŠµē½āŅŗa£»X”¢YŹĒĮ½æéµē¼«°å£¬Ķعżµ¼ĻßÓėÖ±Į÷µēŌ“ĻąĮ¬£®Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
µē½āŌĄķŌŚ»Æѧ¹¤ŅµÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®ČēĶ¼±ķŹ¾Ņ»øöµē½ā³Ų£¬×°ÓŠµē½āŅŗa£»X”¢YŹĒĮ½æéµē¼«°å£¬Ķعżµ¼ĻßÓėÖ±Į÷µēŌ“ĻąĮ¬£®Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ķ¼1±ķŹ¾ĻąĶ¬ĪĀ¶ČĻĀpH=1µÄŃĪĖįŗĶ“×ĖįČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶŹ±pHµÄ±ä»ÆĒśĻߣ¬ĘäÖŠĒśĻߢņĪŖŃĪĖį£¬ĒŅbµćČÜŅŗµÄµ¼µēŠŌ±ČaµćĒæ | |
| B£® | Ķ¼2ÖŠ“æĖ®½öÉżøßĪĀ¶Č£¬¾ĶæÉŅŌ“Óaµć±äµ½cµć | |
| C£® | Ķ¼1ÖŠ£¬bµćĖįµÄ×ÜÅØ¶Č“óÓŚaµćĖįµÄ×ÜÅØ¶Č | |
| D£® | Ķ¼2ÖŠŌŚbµć¶ŌÓ¦ĪĀ¶ČĻĀ£¬½«pH=2µÄH2SO4ÓėpH=10µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗĻŌÖŠŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½CH2CH2 | B£® | ŅŅ“¼µÄ·Ö×ÓŹ½C2H6O | ||
| C£® | ŅŅĖįŅŅÖ¬µÄ½į¹¹¼ņŹ½ŹĒCH3COOC2H5 | D£® | ĖÄĀČ»ÆĢ¼µÄµē×ÓŹ½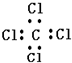 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCl[H2O] | B£® | NaOH[Na2O] | C£® | KI[HI] | D£® | CuSO4[Cu£ØOH£©2] |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×Ķ锢±ūČ² | B£® | ¼×Č©”¢¹ūĢĒ | C£® | ŅŅ“¼”¢ŅŅ¶ž“¼ | D£® | ¼×±½”¢øŹÓĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
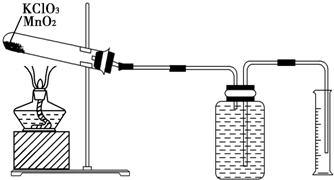
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com