
在2L密闭容器中进行如下反应:N2+3H2 2NH3,5min内氨的质量增加了1.7g,则反应速率为()
2NH3,5min内氨的质量增加了1.7g,则反应速率为()
A. V(NH3)=0.02mol.(L.min)﹣1 B. V(NH3)=0.01mol.(L.min)﹣1
C. V(N2)=0.01mol.(L.min)﹣1 D. V(H2)=0.03mol.(L.min)﹣1
考点: 化学反应速率和化学计量数的关系.
专题: 化学反应速率专题.
分析: 5min内氨的质量增加了1.7g,n(NH3)=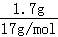 =0.1mol,v(NH3)=
=0.1mol,v(NH3)= =0.01mol.(L.min)﹣1,结合反应速率之比等于化学计量数之比来解答.
=0.01mol.(L.min)﹣1,结合反应速率之比等于化学计量数之比来解答.
解答: 解:A.5min内氨的质量增加了1.7g,n(NH3)=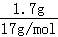 =0.1mol,v(NH3)=
=0.1mol,v(NH3)= =0.01mol.(L.min)﹣1,故A错误;
=0.01mol.(L.min)﹣1,故A错误;
B.5min内氨的质量增加了1.7g,n(NH3)=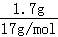 =0.1mol,v(NH3)=
=0.1mol,v(NH3)= =0.01mol.(L.min)﹣1,故B正确;
=0.01mol.(L.min)﹣1,故B正确;
C.反应速率之比等于化学计量数之比,则V(N2)= ×0.01mol.(L.min)﹣1=0.005mol.(L.min)﹣1,故C错误;
×0.01mol.(L.min)﹣1=0.005mol.(L.min)﹣1,故C错误;
D.反应速率之比等于化学计量数之比,则V(H2)= ×0.01mol.(L.min)﹣1=0.015mol.(L.min)﹣1,故D错误;
×0.01mol.(L.min)﹣1=0.015mol.(L.min)﹣1,故D错误;
故选B.
点评: 本题考查化学反应速率的计算及速率与化学计量数的关系,为高频考点,侧重分析能力和计算能力的考查,注意反应速率之比等于化学计量数之比,题目难度不大.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。请完成下列空白:
(1)铝元素在周期表中的位置为________。
(2)在19世纪时,铝是一种珍贵的金属。人们最初得到的铝粒如同珍宝,它的价格同黄金 相当。1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。用钾与无水氯化铝反应制铝而不用氯化铝溶液的理由是_________。
现代工业炼铝的原料是由铝土矿提取而得,在提取过程中通入的气体为____。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高 温下煅烧,所得物质可作耐高温材料,
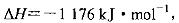 则反应过程中,每转移1 mol电子放出的热量为________。
则反应过程中,每转移1 mol电子放出的热量为________。
(4)硅与铝同周期,地壳里硅铝的含量:硅________铝(填>,<或=)。是硅酸盐玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成 。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
(5)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
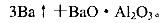 利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
_____________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,由此可判断BeCl2属于( )
A.由极性键形成的极性分子
B.由极性键形成的非极性分子
C.由非极性键形成的极性分子
D.由非极性键形成的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是含碳、氢、氧的单官能团化合物,A水解得B和C,B氧化可以得到C或D,D氧化也得到C。若M(X)表示X的摩尔质量,则下式中正确的是( )
A.M(A)=M(B)+M(C)
B.2M(D)=M(B)+M(C)
C.M(B)<M(D)<M(C)
D.M(D)<M(B)<M(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A、B、C、D、E、F、G相互关系如图所示。5.2 g F能与100 mL 1 mol·L-1的NaOH溶液恰好完全中和,0.1 mol F还能与足量金属钠反应,在标准状况下放出2.24 L H2。D的分子式为C3H3O2Na,E的分子中含有羧基。
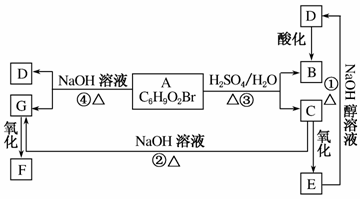
(1)写出下列物质的结构简式:G:________________;F:________________。
(2)化学反应类型:①________________;④________________。
(3)化学方程式:①__________________________;③__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
鉴别FeCl3溶液和Fe(OH)3胶体,下列方法中最简单有效的是()
A. 加入足量的盐酸 B. 加热煮沸
C. 加入足量的NaOH溶液 D. 观察能否产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是()
A. 将过量的二氧化碳通入氢氧化钠溶液:CO2+2OH﹣═CO32﹣+H2O
B. 氯化铝溶液中加入过量浓氨水:Al3++4OH﹣═AlO2﹣+2H2O
C. 氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+
D. 碳酸钙和盐酸反应:CO32﹣+2H+═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
把Ba(OH)2溶液滴入到明矾溶液中,使SO42﹣全部转化成BaSO4沉淀,此时铝元素的主要存在形式是()
A. Al3+ B. Al(OH)3 C. AlO2﹣ D. Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物其结构简式为 ,关于该有机物下列叙述正确的是()
,关于该有机物下列叙述正确的是()
A. 不能使酸性KMnO4溶液褪色
B. 不能使溴水褪色
C. 在加热和催化剂作用下,最多能和4mol H2反应
D. 一定条件下,能和NaOH醇溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com