
【题目】下列事实能证明碳的非金属性比硅强的是
Na2SiO3+CO2+2H2O=H4SiO4↓+Na2CO3 ②SiO2+2C![]() Si+2CO↑
Si+2CO↑
③Na2CO3+SiO2![]() Na2SiO3+CO2↑ ④CH4比SiH4稳定
Na2SiO3+CO2↑ ④CH4比SiH4稳定
A. ①④B. ①②④C. ②④D. ①②③④
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】(1)已知C(s、金刚石)+O2(g)![]() CO2(g);ΔH=-395.4 kJ·mol-1,C(s、石墨)+O2(g)
CO2(g);ΔH=-395.4 kJ·mol-1,C(s、石墨)+O2(g)![]() CO2(g);ΔH=-393.5 kJ·mol-1。
CO2(g);ΔH=-393.5 kJ·mol-1。
①石墨和金刚石相比,石墨的稳定性_________金刚石的稳定性。
②石墨中C-C键键能________金刚石中C-C键键能。(均填“大于” “小于”或“等于”)。
(2)将4g CH4完全燃烧生成气态CO2和液态水,放出热量222.5 kJ,其热化学反应方程式为:______________________________________________________。
(3)0.5mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为:______________________________________________。
(4)已知下列反应的反应热:
CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.2kJ·mol-1
CO(g)+3H2(g) △H1=+206.2kJ·mol-1
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近有研究人员发现了一种处理高浓度乙醛废水的新方法——隔膜电解法,实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,采用如图所示装置电解,电解后乙醛转化为乙醇和乙酸。则下列说法不正确的是( )
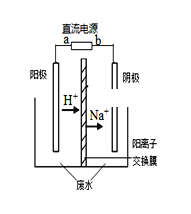
A. 阳极产物为乙酸,发生氧化反应
B. 电解时,阳极区附近pH 增大
C. 阴极反应式为CH3CHO+2H++2e-=CH3CH2OH
D. 若以CH4一空气燃料电池为直流电源,则燃料电池的a 极应通入空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化符合图示的是( )
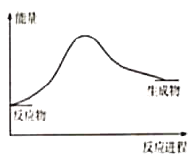
①冰雪融化 ②KMnO4分解制O2 ③铝与氧化铁的反应 ④钠与水反应 ⑤二氧化碳与灼热的木炭反应 ⑥碘的升华 ⑦Ba(OH)2·8H2O和NH4Cl的反应.
A. ②⑥⑦B. ②⑤⑦C. ①②⑤⑥⑦D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,其中离子交换膜I、II分别是氯离子交换膜和钠离子交换膜中的一种,图中有机废水中的有机物可用C6H10O5表示。下列有关说法正确的是

A. a电极为该电池的负极,离子交换膜I是钠离子交换膜
B. a电极附近溶液的氯离子浓度增大,b电极附近溶液的pH减小
C. a电极的电极反应式为C6H10O5-24e-+7H2O=6CO2↑+24H+
D. 中间室中Na+移向左室,Cl—移向右室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N和Si能形成多种高硬度材料,如SiN4、C3N4、SiC
(1)Si3N4和C3N4中硬度较高的是________,理由是_____________。
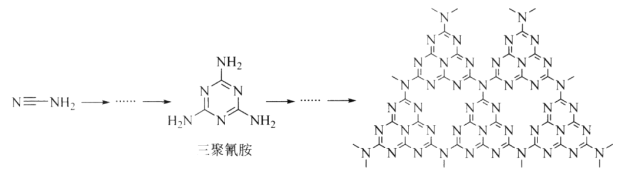
(2)C和N能形成一种类石墨结构材料,其合成过程如下图所示。该类石墨结构材料化合物的化学式为_______,其合成过程中有三聚氰胺形成,三聚氰胺中N原子的杂化方式有________。
(3)C和N能形成一种五元环状有机物咪唑(简写为im),其结构为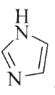 。化合物[Co(im)6]SiF6的结构示意图如下:
。化合物[Co(im)6]SiF6的结构示意图如下:
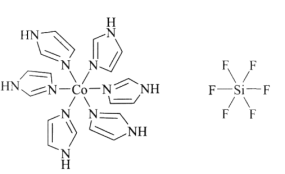
①阳离子[Co(im)6]2+和SiF62—之间除了阴阳离子间的静电作用力,还存在氢键作用写出该氢键的表示式:_______。(例如水中氢键的表示式为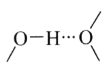 )
)
②多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如SO2分子中存在“离域π键” π34,则im分子中存在的“离域π键”是______。
(4)![]() -SiC为立方晶系晶体,该晶胞中原子的坐标参数为
-SiC为立方晶系晶体,该晶胞中原子的坐标参数为
C:(0,0,0);![]() ;
;![]() ;
;![]() ;……
;……
Si:![]() ;
;![]() ;
;![]() ;
;![]()
则![]() -SiC立方晶胞中含有_____个Si原子、________个C原子。
-SiC立方晶胞中含有_____个Si原子、________个C原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学拟通过实验探究同主族元素性质的递变规律。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:NaBr溶液、NaI溶液、新制的氯水
(1)写出下列实验报告中的实验现象和离子方程式
实验步骤 | 实验现象 | 实验结论及离子方程式 |
| 甲_______ 乙_______ | 离子方程式 甲__________ 乙__________ 结论:卤素单质的氧化性由强到弱的顺序为Cl2>Br2>I2 |
(2)[评价]甲同学设计的实验方案的合理性是_____(填字母)。
A.非常合理 B.部分合理 C.完全不合理
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com