
 ,该反应生成硝酸盐、NO,可体现硝酸的酸性、强氧化性,生成2molNO转移6mol电子,对应2mol硝酸被还原,则当被还原的硝酸是0.1mol时,生成的NO的体积0.1mol×22.4L/mol=2.24L,
,该反应生成硝酸盐、NO,可体现硝酸的酸性、强氧化性,生成2molNO转移6mol电子,对应2mol硝酸被还原,则当被还原的硝酸是0.1mol时,生成的NO的体积0.1mol×22.4L/mol=2.24L, ;酸;强氧化;2.24L.
;酸;强氧化;2.24L.


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
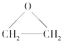 ),该反应的原子利用率为100%,反应的化学方程式为
),该反应的原子利用率为100%,反应的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三氯化铁溶液中加入NaOH溶液出现红褐色沉淀 |
| B、煮沸的 FeCl3溶液冷却后,用一束光照射,有一条光的通路 |
| C、胶态金属氧化物分散于玻璃中制成有色玻璃 |
| D、明矾可以用来净水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com