
同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳,下列说法正确的是( )
A.所含分子数和质量均不相同
B.含有相同的分子数和电子数
C.含有相同的质子数和中子数
D.含有相同数目的中子、原子和分子
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
下列排列顺序正确的是( )
A.粒子半径:Al3+>Mg2+>F-
B.热稳定性:HI>HBr>HCl>HF
C.酸性:H2SiO3<H3PO4<H2SO4<HClO4
D.碱性:Al(OH)3>Mg(OH)2>NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
已知N2和H2合成氨的反应是放热反应,破坏1 mol N≡N键消耗的能量为Q1kJ,破坏1 mol H—H键消耗的能量为Q2kJ,形成1 mol N—H键放出的能量为Q3kJ,下列关系式中正确的是 ( )
A.Q1+3Q2>6Q3 B.Q1+3Q2<6Q3
C.Q1+Q2<Q3 D.Q1+Q2=Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2A===B+D在四种不同条件下进行。B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | 温度 | 0 min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20 min时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=______mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是____________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______v1(填“>”、“=”或“<”),且c3______1.0 mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”或“放热”),理由是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是 ( )
A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列具有特殊性能的材料中,由主族和副族元素组成的是( )
A.半导体材料砷化镓
B.吸氢材料镧镍合金
C.透明陶瓷材料硒化锌
D.新型纳米材料氮化镓
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.061 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图,下列对该化合物叙述正确的是( )
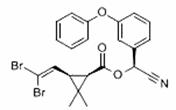
A.属于芳香烃 B.属于卤代烃 C.属于高分子化合物 D.属于有机化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(白磷,s)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1①
P(红磷,s)+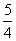 O2(g)===
O2(g)===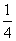 P4O10(s) ΔH2=-738.5 kJ·mol-1②
P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为____________________________。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com