


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、2NO(g)+O2(g)?2NO2(g) |
| B、N2O4 (g)?2NO2(g) |
| C、Br2(g)+H2(g)?2HBr(g) |
| D、6NO(g)+4NH3(g)?5N2(g)+3H2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为
(1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| 一定条件 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
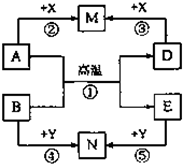 构建知识网络是学习化学的重要方法.下列物质的转化网络可以概括几类反应,其中A、B、D、E、M、N、X、Y均表示一种中学化学中常见的无机物,反应②、③、④、⑤的生成物可以是一种或几种.请回答下列问题:
构建知识网络是学习化学的重要方法.下列物质的转化网络可以概括几类反应,其中A、B、D、E、M、N、X、Y均表示一种中学化学中常见的无机物,反应②、③、④、⑤的生成物可以是一种或几种.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- |
| B、将氯气通入KI溶液中:Cl2+2I-═2Cl-+I2 |
| C、将氯气通入水中:Cl2+H2O═Cl-+ClO-+2H+ |
| D、将锌粒投入稀硝酸中:Zn+2H+=Zn2++H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com