
A、
| ||
B、
| ||
C、
| ||
D、
|
| r(K+) |
| r(Na+) |
| r(Be) |
| r(Mg) |
| r(P) |
| r(Si) |
| r(Cl) |
| r(Cl-) |


科目:高中化学 来源: 题型:
| A、在氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
| B、在硝酸银溶液中滴入氯化钠溶液:Ag++Cl-=AgCl↓ |
| C、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化石燃料在任何条件下都能充分燃烧 |
| B、化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| C、直接燃烧煤不如将煤进行深加工后,再燃烧效果好 |
| D、固体煤变为气体燃料后,燃烧效率将更高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠是银白色金属,熔点低,硬度大 |
| B、钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠 |
| C、加热时,金属钠剧烈燃烧,产生黄色火焰 |
| D、金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强酸溶液中的氢离子浓度一定大于弱酸溶液中的氢离子浓度 |
| B、NaOH溶液的导电性一定比氨水的导电性强 |
| C、不溶性盐都是弱电解质,可溶性酸都是强电解质 |
| D、二氧化硫和乙醇均属共价化合物,是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
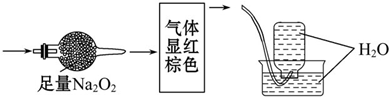
| A、NO2、N2 |
| B、NO、CO2 |
| C、NO2、CO2 |
| D、NO、CO2、N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com