
| A. | 当x≤4时,常温、常压下均为气体 | |
| B. | y一定是偶数 | |
| C. | 将烃燃烧1 mol,耗氧气为(x+$\frac{y}{4}$)mol | |
| D. | 在密闭容器中完全燃烧,120℃时测得的压强一定比燃烧前增加 |
分析 A.烷、烯、炔烃中,碳原子数≤4时,常温下一般为气体;
B.根据烷、烯、炔烃的通式进行判断;
C.完全燃烧时,1molC原子消耗1mol氧气、1mol氢原子消耗$\frac{1}{4}$mol氧气,所以1molCxHy完全燃烧消耗(x+$\frac{y}{4}$)mol氧气;
D.120℃时水为气体,根据CxHy燃烧的通式对气体体积变化进行判断.
解答 解:A.对应烷烃、烯烃和炔烃中,碳原子数目≤4时,常温下都是气体,故A正确;
B.烷、烯、炔烃分子中,烷烃的通式是CnH2n+2,单烯烃的通式是CnH2n(若是多个双键,则每多一个双键,H的个数减少2,因此氢数一定是偶数),炔烃的推断过程和烯烃类似,故B正确;
C.烃燃烧时,1molC原子消耗1mol氧气、1mol氢原子消耗$\frac{1}{4}$mol氧气,所以1molCxHy完全燃烧消耗(x+$\frac{y}{4}$)mol氧气,故C正确;
D、120℃时水的状态为气体,1molCxHy完全燃烧消耗(x+$\frac{y}{4}$)mol氧气,同时生成xmol二氧化碳、$\frac{y}{2}$mol水,当满足:1+(x+$\frac{y}{4}$)<x+$\frac{y}{2}$,即y>4时,反应后气体总压强增加,故D错误;
故选D.
点评 本题主要考查了常见有机物的组成与性质,题目难度中等,注意掌握烷、烯、炔烃的组成与性质,明确常温下呈气态的烃的情况,能够根据烃的燃烧通式判断其燃烧情况.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
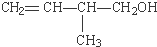 的键线式
的键线式
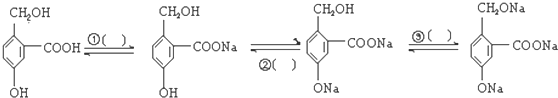
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl是取代反应 | |
| B. | CH2=CH2+Br2→CH2Br-CH2Br是加成反应 | |
| C. | 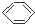 +HO-NO2$→_{60℃}^{浓硫酸}$ +HO-NO2$→_{60℃}^{浓硫酸}$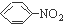 +H2O是取代反应 +H2O是取代反应 | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
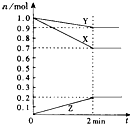 (1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:3X+Y
(1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:3X+Y 2Z
2Z查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com