
| A. | 1mol任何物质都含有6.02×1023个分子 | |
| B. | 在相同条件下,相同物质的量CO、N2的混合气体与O2的分子个数相同,原子个数也相同 | |
| C. | NaOH的摩尔质量40g | |
| D. | 在标准状况下,1molO2与1molSO3的体积相同 |
分析 A.原子晶体、离子晶体及金属晶体中不存在分子;
B.三种气体都是双原子分子中,根据N=nNA分析;
C.摩尔质量的单位为g/mol;
D.标准状况下三氧化硫的状态不是气体.
解答 解:A.有些物质中不含有分子,如原子晶体、离子晶体及金属晶体,则1mol物质中不一定含有6.02×1023个分子,故A错误;
B.由于单质都是双原子分子,则在相同条件下,相同物质的量CO、N2的混合气体与O2的分子个数、原子个数都相同,故B正确;
C.NaOH的摩尔质量应该为40g/mol,故C错误;
D.标况下氧气为气体,而三氧化硫为固体,则标况下1molO2与1molSO3的体积不相同,故D错误;
故选B.
点评 本题考查物质的量的计算,题目难度不大,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与其它物理量之间的关系,试题培养了学生的分析能力及灵活应用能力.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:选择题
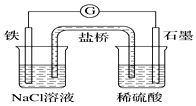
| A. | 石墨电极上发生氧化反应 | B. | 负极反应:2H++2e-═H2↑ | ||
| C. | 电流方向:石墨→铁 | D. | 盐桥中Cl-向右池移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
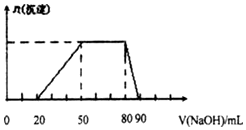 某50mL溶液中可能含有H+、Na+、Mg2+、Al3+、SO42-、NH4+离子,当向该溶液中加入5mol/L的NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积v(NaOH)变化关系如图所示.( )
某50mL溶液中可能含有H+、Na+、Mg2+、Al3+、SO42-、NH4+离子,当向该溶液中加入5mol/L的NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积v(NaOH)变化关系如图所示.( )| A. | 原溶液中一定含有的阳离子是H+、Mg2+、Al3+ | |
| B. | 原溶液中Al3+的浓度为lmol/L | |
| C. | 原溶液中NH4+的物质的量为0.4 mol | |
| D. | 当加入的NaOH溶液的体积为90mL时,反应后溶液中的离子只有Na+和SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴入甲基橙显红色的溶液中:Al3+、NH4+、SO42-、MnO4- | |
| B. | 在酸性KMnO4溶液中:SO42-、Mg2+、NO3-、CH3CH2OH | |
| C. | 常温下由水电离出的c(H+)•c(OH-)=10-20 mol2•L-2的溶液中:Na+、NH4+、Cl-、SiO32- | |
| D. | 使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 3种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com