
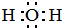 ,HCl中的化学键类型是共价键.
,HCl中的化学键类型是共价键.分析 (1)根据H2O为共价化合物书写电子式,HCl为非金属之间形成的共价键;
(2)反应热△H=反应物总键能-生成物的总键能,据此计算H-O键与H-Cl键的键能差,进而计算断开1mol H-O键与断开1mol H-Cl键所需能量差.
解答 解:(1)因为H2O为共价化合物,则H2O的电子式为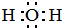 ,HCl为非金属之间形成的共价键,故答案为:
,HCl为非金属之间形成的共价键,故答案为: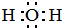 ;共价键;
;共价键;
(2)E(H-O)、E(H-Cl)分别表示H-O键能、H-Cl键能,
反应中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:
4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+4×E(H-O)]=-115.6kJ/mol,
整理得,4E(H-Cl)-4E(H-O)=-127.6kJ/mol,即E(H-O)-E(HCl)=31.9kJ/mol,故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ/mol×1mol=31.9kJ≈32kJ,更稳定的化学键是H-O;故答案为:32kJ;H-O.
点评 本题考查了焓变、焓变等于反应物的键能和减去生成物的键能和,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 正确操作步骤的顺序是⑤②③①④ | |
| B. | 步骤④电解时阴极产生氯气 | |
| C. | 直接在空气中将MgCl2溶液蒸干可得到Mg(OH)2 | |
| D. | 此法提取镁的过程中涉及置换、分解、化合和复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3(两性氧化物) | B. | H2SO4(含氧酸) | C. | CH3COOH(烃) | D. | 食醋(混合物) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)2003年夏,全球化学家投票评选了化学史上十项最美的实验,1848年巴斯德用手工在光学显微镜下把左型酒石酸盐晶体和右型酒石酸盐晶体分开的实验被选为十项之首.请回答下列问题:
(1)2003年夏,全球化学家投票评选了化学史上十项最美的实验,1848年巴斯德用手工在光学显微镜下把左型酒石酸盐晶体和右型酒石酸盐晶体分开的实验被选为十项之首.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与1molFe反应,转移的电子数为3NA | |
| B. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA | |
| C. | 在标准状况下,Cl2和H2的混合气22.4升,光照后原子总数为2NA | |
| D. | 0.1mol•L-1的FeCl3溶液中含有0.1NA个Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com