
【题目】(1)HCl、NH4Cl、CH3COOH和CH3COONa是中学常见的物质。
①常温下在pH=7的CH3COOH和CH3COONa的混合液中c(Na+)_______c(CH3COO-)(填“>”、“<”或“=”);
②常温下pH均为6的HCl和NH4Cl两种溶液中,设由水电离产生的H+浓度分别为amol/L和bmol/L,则a与b的关系是_______;
A.a=b B.a=100b C.b=100a
(2)T℃,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C物质的量变化如图所示。

①T℃时,该反应的化学方程式为________;
②0~4分钟时,A的平均反应速率为_______molL-1min-1;
③达到平衡时B的转化率为________;
④T℃时,该反应的平衡常数为________。
(3)将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一。
已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)ΔH=+140.5kJ/mol
C(s,石墨)+![]() O2(g)=CO(g) ΔH=-110.5kJ/mol
O2(g)=CO(g) ΔH=-110.5kJ/mol
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(l)+2CO(g)的ΔH是_______。
A.+80.5kJ/mol B.+30.0kJ/mol
C.-30.0kJ/mol D.-80.5kJ/mol
(4)Cu(OH)2在水溶液中存在溶解平衡:Cu(OH)2(s)![]() Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)c2(OH-)=2×10-20。当溶液中各离子浓度幂的乘积大于溶度积时,则产生沉淀,反之无沉淀。某CuSO4溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH>________。
Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)c2(OH-)=2×10-20。当溶液中各离子浓度幂的乘积大于溶度积时,则产生沉淀,反之无沉淀。某CuSO4溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH>________。
(5)茫茫黑夜中,航标灯为航海员指明了方向.航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。
①该电池中,海水是电解质溶液,负极材料_______(填“铝合金”或“Pt-Fe合金网”);
②该电池中负极电极反应式为_______。
【答案】= C 2A+B![]() C 0.05 25% 0.52 D 5 铝合金 Al-3e-=Al3+
C 0.05 25% 0.52 D 5 铝合金 Al-3e-=Al3+
【解析】
(1)①根据电荷守恒CH3COOH和CH3COONa的混合液中c(Na+)+ c(H+)=c(CH3COO-)+ c(OH-),pH=7的溶液,c(H+)=c(OH-),所以c(Na+)=c(CH3COO-);
②HCl抑制水电离,常温下pH为6的HCl,由水电离产生的H+浓度等于OH-的浓度,由水电离产生的H+浓度等于![]() mol/L;NH4Cl水解促进水电离,常温下pH为6的NH4Cl,由水电离产生的H+浓度等于
mol/L;NH4Cl水解促进水电离,常温下pH为6的NH4Cl,由水电离产生的H+浓度等于![]() mol/L,所以b=100a,选C;
mol/L,所以b=100a,选C;
(2)①A、B的物质的量减少、C的物质的量增加,A、B是反应物、C是生成物,0到t3时刻,A的变化量是0.8mol、B的变化量是0.4mol,C的变化量是0.4mol,变化量比等于系数比,所以反应方程式是2A+B![]() C;
C;
②v(A)=![]() 0.05 mol·L-1·min-1;
0.05 mol·L-1·min-1;
③达到平衡时B的转化率=变化量/初始量×100%=(1.6-1.2)/1.6×100%=25%;
④T℃时,该反应的平衡常数=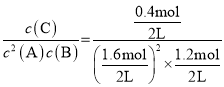 =0.52;
=0.52;
(3)①TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)ΔH=+140.5kJ/mol
②C(s,石墨)+![]() O2(g)=CO(g) ΔH=-110.5kJ/mol
O2(g)=CO(g) ΔH=-110.5kJ/mol
根据盖斯定律①+②×2得TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(l)+2CO(g),ΔH=+140.5kJ/mol -110.5kJ/mol×2=-80.5kJ/mol,选D;
(4)c(Cu2+)c2(OH-)>2×10-20时生成沉淀,c(Cu2+)=0.02mol/L,则c2(OH-)>![]() ,c(OH-)>
,c(OH-)>![]() mol/L,所以应调整溶液pH>5;
mol/L,所以应调整溶液pH>5;
(5)原电池中活泼金属作负极,铝的活泼性大于铁,所以负极材料是铝合金;负极Al失电子生成Al3+,电极反应为Al-3e-=Al3+。


科目:高中化学 来源: 题型:
【题目】可逆反应2SO2+ O2![]() 2SO3达到平衡的标志是
2SO3达到平衡的标志是
①消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A.①②B.①③C.只有③D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖
B.室温下,将![]() HA溶液和
HA溶液和![]() 溶液等体积混合
溶液等体积混合![]() 忽略体积的变化
忽略体积的变化![]() 测得混合溶液的
测得混合溶液的![]() ,则混合溶液中由水电离出的
,则混合溶液中由水电离出的![]()
C.纯碳新材料“碳纳米泡沫”,每个泡沫含有约4000个碳原子,直径约6到9nm,在低于![]() 时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
D.已知![]() 的
的![]() 为
为![]() ,则将等体积的
,则将等体积的![]()
![]() 的
的![]() 溶液和
溶液和![]()
![]()
![]() 溶液混合后会有
溶液混合后会有![]() 沉淀产生
沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用![]() 溶液分别滴定
溶液分别滴定![]() 溶液和
溶液和![]() 溶液,得到2条滴定曲线,如下图所示:
溶液,得到2条滴定曲线,如下图所示:
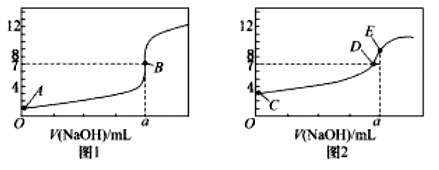
![]() 由A、C点判断,滴定HCl溶液的曲线是_____
由A、C点判断,滴定HCl溶液的曲线是_____![]() 填“图1”或“图2”
填“图1”或“图2”![]() ;
;
![]()
![]() ____
____![]() ;
;
![]()
![]() 的点是_________;
的点是_________;
![]() 点对应离子浓度由大到小的顺序为___________________________。
点对应离子浓度由大到小的顺序为___________________________。
![]() 当NaOH溶液滴定
当NaOH溶液滴定![]() 溶液过程中,NaOH溶液消耗了
溶液过程中,NaOH溶液消耗了![]() mL时,则此时混合液中
mL时,则此时混合液中![]() ____c
____c![]() “
“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() 。
。
![]() 室温时,浓度均为
室温时,浓度均为![]() 的
的![]() 和NaOH的混合液
和NaOH的混合液![]() ,则溶液中
,则溶液中![]() ___________
___________![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol·L-1Na2SO4溶液,下列叙述正确的是
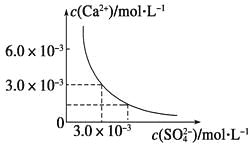
A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的叙述正确的是( )
A.丙烷的二卤代物是4种,则其六卤代物是2种
B.某烃的同分异构体只能形成一种一氯代物,其分子式一定为C5H12
C.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
D.对二甲苯的核磁共振氢谱显示有3种不同化学环境的氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-8mol·L-1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分利用能源,提高原子利用率,减少向环境排放废弃物等都是“绿色化学”![]() 基本要求。下述做法主要是从“绿色化学”角度考虑的是( )
基本要求。下述做法主要是从“绿色化学”角度考虑的是( )
①实验室短时间保存硫酸亚铁溶液时,向试剂瓶中添加少量铁粉;②用稀硝酸代替浓硝酸溶解、回收做银镜实验后试管内壁的银;③用印刷电路的废液溶解废铁屑制氯化亚铁并回收铜;④工业合成氨中分离产物得到氢气和氮气再循环使用。
A.①③④B.②③④C.①②④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示的装置制取乙酸乙酯,下列说法中不正确的是( )
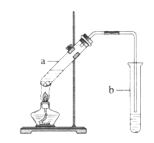
A.及时将乙酸乙酯蒸出,平衡向生成乙酸乙酯的方向移动
B.向试管a中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
C.试管b中导气管下端不能浸入液面的目的是防止实验过程中产生倒吸现象
D.反应结束后用分液的方法分离试管b中的混合液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com