
【题目】(1)某学习小组利用下图装置制取氯气并探究其性质。
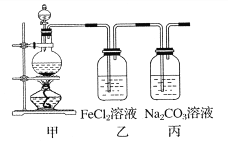
①甲装置中反应的化学方程式是_____________________________________;
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象)__________________________________________________________;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是____________________________________。
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究。
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol·L-1盐酸、品红溶液、新制澄清石灰水。
(提出假设)假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含________________;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3 。
(进行实验)在答题卡上完成下表(不必检验Ca2+、Cl-):
实验步骤 | 预期现象和结论 | |
① | 用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管___________________________ | 若无气体放出且澄清石灰水未见浑浊,则假设一成立;______________________________ |
② | __________________________ | ___________________________________________ |
【答案】MnO2+4HCl (浓)![]() MnCl2+ Cl2↑+2H2O KSCN溶液溶液变红色或NaOH溶液,红褐色沉淀等合理答案 Cl2+2H2O+Na2CO3=NaCl+NaCl+2NaHCO3 CaCO3 CaCl2 加入适量1mol/L-1盐酸,塞上带导管的单孔塞,将导管另一端插入A试管中 若有气体放出且澄清石灰水变浑浊,则假设二或三成立 用胶头滴管向上述步骤后的B试管中滴入几滴品红溶液,振荡[或另取少量样品于试管中,滴入几滴蒸馏水振荡,再滴入品红溶液] 若品红不褪色,则假设二成立;若品红褪色,假设三成立
MnCl2+ Cl2↑+2H2O KSCN溶液溶液变红色或NaOH溶液,红褐色沉淀等合理答案 Cl2+2H2O+Na2CO3=NaCl+NaCl+2NaHCO3 CaCO3 CaCl2 加入适量1mol/L-1盐酸,塞上带导管的单孔塞,将导管另一端插入A试管中 若有气体放出且澄清石灰水变浑浊,则假设二或三成立 用胶头滴管向上述步骤后的B试管中滴入几滴品红溶液,振荡[或另取少量样品于试管中,滴入几滴蒸馏水振荡,再滴入品红溶液] 若品红不褪色,则假设二成立;若品红褪色,假设三成立
【解析】
(1)①甲装置是制取氯气的装置发生的反应是二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水的反应;
②氯化铁遇到硫氰酸钾溶液会发生反应生成血红色溶液;
③氯气和水反应生成盐酸和次氯酸,盐酸和足量碳酸钠反应生成氯化钠和碳酸氢钠,次氯酸和碳酸钠反应生成次氯酸钠和碳酸氢钠;
(2)漂白粉的主要成分为CaCl2、Ca(ClO)2,Ca(ClO)2易与空气中二氧化碳和水反应生成HClO,HClO不稳定,见光分解生成HCl和水,最终生成CaCl2、CaCO3,如果漂白粉部分变质,则成分为CaCl2、Ca(ClO)2、CaCO3,检验是否变质可根据碳酸钙和盐酸反应生成二氧化碳气体,能使澄清石灰水变浑浊,次氯酸钙和盐酸反应生成氯气,能使品红褪色,通过这两个实验检验漂白粉变质程度。
(1)①浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
②氯化铁和氯气反应,2FeCl2+Cl2=2FeCl3,三价铁离子和硫氰酸钾反应生成血红色溶液,Fe3++3SCN-=Fe(SCN)3;
故答案为:KSCN,溶液变为血红色;
③氯气和水反应生成盐酸和次氯酸,盐酸和足量碳酸钠反应生成氯化钠和碳酸氢钠,次氯酸和碳酸钠反应生成次氯酸钠和碳酸氢钠,所以方程式为Cl2+2Na2CO3+H2O=NaCl+NaClO+2NaHCO3;
故答案为:Cl2+2Na2CO3+H2O=NaCl+NaClO+2NaHCO3;
(2)漂白粉的主要成分为CaCl2、Ca(ClO)2,Ca(ClO)2易与空气中二氧化碳和水反应生成HClO,HClO不稳定,见光分解生成HCl和水,最终生成CaCl2、CaCO3;如漂白粉没有变质,则漂白粉中无CaCO3,加入盐酸后无气体放出且澄清石灰水未见浑浊;如漂白粉全部变质,则产物为CaCl2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,则品红不褪色,而石灰水变浑浊;如漂白粉部分变质,漂白粉中含有CaCl2、Ca(ClO)2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水变浑浊;
故答案为:CaCl2、CaCO3;
实验步骤 | 预期现象和结论 | |
① | 再向B试管加入1mol/L的稀盐酸加入适量1mol/L的盐酸,塞上带导管的单孔塞,将导管的另一端插入A试管中 | 若有气泡冒出,且澄清石灰水变浑浊则假设一不成立,假设二、三成立 |
② | 用胶头滴管向上述步骤后的B试管中滴入几滴品红试液,振荡 | 若品红溶液不褪色,则假设二成立,若品红溶液褪色,则假设三成立 |


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】PETG是一种新型材料,可回收利用,对环境不构成任何威胁,其结构简式如下: ,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:
,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:

试回答下列问题:
(1)试剂X为______________;反应⑦的反应类型为_______________。
(2)写出物质H的名称________________________。
(3)写出结构简式: I_____________________________。
(4)写出反应⑤的化学方程式:_________________________________________。
(5)合成时应控制的单体的物质的量n (D)∶n (F)∶n (H)=__________(用m、n表示)。
(6)同时符合下列要求的物质H的同分异构体共有__________种。
①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应,并有气体放出;③能发生银镜反应。
(7)已知:![]() 请写出由D及其它必要物质可合成
请写出由D及其它必要物质可合成![]() 的反应历程。________________
的反应历程。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两池中的电极材料都是铁棒与碳棒,请回答下列问题。
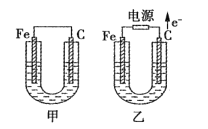
(1)若两池中的电解质溶液均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的__棒,乙池中的__棒。
②乙池中阳极的电极反应式是__。
(2)若两池中的电解质溶液均为饱和NaCl溶液:
①乙池中总反应的离子方程式为__。
②乙池中碳棒上的电极反应属于__(填“氧化反应”或“还原反应”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求,回答下列问题:
(1)下列现象和应用与电子跃迁无关的是___。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用__形象化描述。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)__I1(Cu)(填“大于”或“小于”)。原因是__。
(4)ZnF2具有较高的熔点(872℃),其化学键类型是___;
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为___,![]() 原子的杂化形式为__。
原子的杂化形式为__。
(6)与H2O分子互为等电子体的阴离子为__。
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为__。
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为__kJ/mol。ClF3的熔、沸点比BrF3的__(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分难溶物的颜色和常温下的Ksp如下表所示:
Cu(OH)2 | CuOH | CuCl | Cu2O | |
颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
Ksp(25 ℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | — |
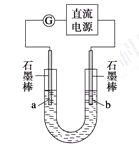
某研究性学习小组对电解食盐水进行了如下探究:
实验Ⅰ装置如图所示,接通电源后,发现a、b电极上均有气泡产生。
(1)电解过程中的总离子反应方程式为_________________________________________。
(2)为了确定电源的正、负极,下列操作一定行之有效的是_______。
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示。

观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色。
(3) a极发生的电极反应方程式为________________________________________________________。
(4) 电解5 min后,b极发生的电极反应方程式为___________________________________________。
(5)12 min后,b极附近出现的橙黄色沉淀的成分是_____,原因是___________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以证明2HI(g)![]() H2(g)+I2(g)已达平衡状态的是( )
H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②一个H—H键断裂的同时有两个H—I键断裂
③温度和体积一定时,混合气体密度不再变化
④v(H2)=v(I2)=0.5v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和压强一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
A. ②③④⑤⑥B. ②⑥⑦⑧⑨
C. ①②⑥⑧D. ②⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)=C(石墨)![]() <0,可知,金刚石比石墨稳定
<0,可知,金刚石比石墨稳定
C.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ![]() = -571.6kJ/mol
= -571.6kJ/mol
D.在稀溶液中,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是

A. 图甲表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B. 图乙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,乙的压强比甲的压强大
3C(g)+D(g)的影响,乙的压强比甲的压强大
C. 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com