
分析 (1)草酸的酸性比碳酸强,故草酸与碳酸氢钠反应生成二氧化碳,由于草酸足量,故生成NaHC2O4;
(2)2.52g草酸晶体(H2C2O4•2H2O)的物质的量为$\frac{2.52g}{126g/mol}$=0.02mol,NaOH的物质的量为0.1L×0.2mol/L=0.02mol,二者正好1:1反应生成NaHC2O4,溶液显酸性,说明HC2O4-的电离程度大于其水解程度;A.根据电荷守恒判断;
B.根据物料守恒可知,溶液中草酸、醋酸根、草酸氢根的总浓度为0.2mol/L;
C.HC2O4-的电离程度大于其水解程度;
D.根据Na元素与C元素比例关系(物料守恒)判断;
(3)草酸被氧化为二氧化碳,把MnO4-还原为Mn2+,说明草酸具有还原性;
(4)等体积、等pH的盐酸溶液和乙二酸(HOOC-COOH)溶液中氢离子浓度相同;乙二酸是弱酸,盐酸是强酸,加水稀释乙二酸电离被促进.
解答 解:(1)草酸的酸性比碳酸强,故草酸与碳酸氢钠反应生成二氧化碳,由于草酸足量,故还生成NaHC2O4,反应离子方程式为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O,
故答案为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O;
(2)2.52g草酸晶体(H2C2O4•2H2O)的物质的量为$\frac{2.52g}{126g/mol}$=0.02mol,NaOH的物质的量为0.1L×0.2mol/L=0.02mol,二者正好1:1反应生成NaHC2O4,溶液显酸性,说明HC2O4-的电离程度大于其水解程度.
A.根据电荷守恒:c(Na+)+c(H+)═c(HC2O4-)+c(OH-)+2c(C2O42-),故A错误;
B.反应后的溶液为0.2mol/L NaHC2O4溶液,由物料守恒可知,溶液中c(HC2O4-)+c(C2O42-)+c(H2C2O4)═0.2mol/L,故B错误;
C.HC2O4-的电离程度大于其水解程度,且电离程度不大,则溶液中c(HCO4-)>c( C2O42-)>c(H2C2O4),故C正确;
D.反应后的溶液为0.2mol/L NaHC2O4溶液,由钠元素与碳元素关系,可知溶液中c(Na+)═c(H2C2O4)+c( HC2O4-)+c(C2O42-),故D正确,
故答案为:CD;
(3)草酸被氧化为二氧化碳,把MnO4-还原为Mn2+,说明草酸具有还原性,反应离子方程式为:5H2C2O4+6H++2MO4-═2Mn2++10CO2↑+8H2O,
故答案为:还原性;5H2C2O4+6H++2MO4-═2Mn2++10CO2↑+8H2O;
(4)分别向等体积、等pH的盐酸溶液和乙二酸(HOOC-COOH)溶液中:加入足量的Zn粉,反应刚开始时溶液中氢离子浓度相同,所以产生H2速率相同,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH 值仍相同,乙二酸是弱酸,盐酸是强酸,加水稀释乙二酸电离被促进,稀释乙二酸需要加入的水多,则m和n 的关系是m小于n,
故答案为:相同;m小于n.
点评 本题比较综合,涉及离子方程式书写、微粒浓度比较、弱电解质的电离、氧化还原反应等,属于拼合型题目,(1)为易错点,学生容易忽略草酸过量问题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 溴化钾溶液跟适量氯水反应 Cl2+2Br-═Br2+2Cl- | |
| B. | 碳酸钠溶液跟足量盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| C. | 将铁粉放入稀盐酸中 Fe+2H+═Fe2++H2↑ | |
| D. | 将金属钠放入水中 Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
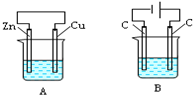 如图所示,A、B两个装置中两个烧杯分别盛有足量的CuSO4溶液:
如图所示,A、B两个装置中两个烧杯分别盛有足量的CuSO4溶液:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=11的Na0H和Na2S溶液中水的电离程度前者大于后者 | |
| B. | 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉 | |
| C. | 25℃,Cu(OH)2在水中的溶度积和溶解度比其在Cu(NO3)2溶液中的大 | |
| D. | 向FeCl3+3KSCN?Fe(SCN)3+3KCl平衡体系中加入少量KCl 固体,溶液血红色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com