
·ÖĪö £Ø1£©ŌŚĖ®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀÄܵ¼µēµÄ»ÆŗĻĪļĪŖµē½āÖŹ£»
£Ø2£©ŌŚĖ®ČÜŅŗÖŠŗĶČŪȌדĢ¬ĻĀ¾ł²»Äܵ¼µēµÄ»ÆŗĻĪļĪŖ·Ēµē½āÖŹ£»
£Ø3£©ÓŠ×ŌÓÉŅĘ¶ÆµÄµē×Ó»ņĄė×ÓµÄĪļÖŹÄܵ¼µē£®
½ā“š ½ā£ŗ¢ŁŹÆÄ«ŹĒµ„ÖŹ£¬Äܵ¼µē£¬¼Č²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ£»
¢ŚNa2O¹ĢĢå²»Äܵ¼µē£¬ŹĒµē½āÖŹ£»
¢ŪŃĪĖįŹĒ»ģŗĻĪļ£¬Äܵ¼µē£¬¼Č²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ£»
¢ÜSO2ŹĒ·Ēµē½āÖŹ£¬²»Äܵ¼µē£»
¢ŻµØ·Æ¾§Ģå²»Äܵ¼µē£¬ŹĒµē½āÖŹ£»
¢ŽĢ¼ĖįøĘ¹ĢĢå²»Äܵ¼µē£¬ŹĒµē½āÖŹ£»
¢ßÕįĢĒ¾§Ģå²»Äܵ¼µē£¬ŹĒ·Ēµē½āÖŹ£»
¢ąNaClČÜŅŗÄܵ¼µē£¬¼Č²»ŹĒ·Ēµē½āÖŹŅ²²»ŹĒµē½āÖŹ£®
£Ø1£©ŌŚĖ®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀÄܵ¼µēµÄ»ÆŗĻĪļĪŖµē½āÖŹ£¬¹ŹŹĒµē½āÖŹµÄŹĒ¢Ś¢Ż¢Ž£¬¹Ź“š°øĪŖ£ŗ¢Ś¢Ż¢Ž£»
£Ø2£©ŌŚĖ®ČÜŅŗÖŠŗĶČŪȌדĢ¬ĻĀ¾ł²»Äܵ¼µēµÄ»ÆŗĻĪļĪŖ·Ēµē½āÖŹ£¬¹ŹŹĒ·Ēµē½āÖŹµÄŹĒ¢Ü¢ß£¬¹Ź“š°øĪŖ£ŗ¢Ü¢ß£»
£Ø3£©ÓŠ×ŌÓÉŅĘ¶ÆµÄµē×Ó»ņĄė×ÓµÄĪļÖŹÄܵ¼µē£¬¹ŹÄܵ¼µēµÄŹĒ¢Ł¢Ū¢ą£¬¹Ź“š°øĪŖ£ŗ¢Ł¢Ū¢ą£®
µćĘĄ ±¾Ģāæ¼²éĮĖµē½āÖŹ”¢·Ēµē½āÖŹŗĶĪļÖŹÄÜ·ńµ¼µēµÄÅŠ¶Ļ£¬ÄŃ¶Č²»“ó£¬Ó¦×¢ŅāµÄŹĒÄܵ¼µēµÄ²»Ņ»¶ØŹĒµē½āÖŹ£¬µē½āÖŹ²»Ņ»¶ØÄܵ¼µē£®


 ĢŅĄīĪÄ»ÆæģĄÖŹī¼ŁĪäŗŗ³ö°ęÉēĻµĮŠ“š°ø
ĢŅĄīĪÄ»ÆæģĄÖŹī¼ŁĪäŗŗ³ö°ęÉēĻµĮŠ“š°ø ÓÅŠćÉśæģĄÖ¼ŁĘŚĆæŅ»ĢģČ«ŠĀŗ®¼Ł×÷Ņµ±¾ĻµĮŠ“š°ø
ÓÅŠćÉśæģĄÖ¼ŁĘŚĆæŅ»ĢģČ«ŠĀŗ®¼Ł×÷Ņµ±¾ĻµĮŠ“š°ø Źī¼Ł½ÓĮ¦ČüŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł½ÓĮ¦ČüŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉÄę·“Ó¦ŹĒÖøŌŚĶ¬Ņ»Ģõ¼žĻĀÄÜĶ¬ Ź±ĻņÕżÄęĮ½øö·½Ļņ½ųŠŠµÄ·“Ó¦ | |
| B£® | 2HI$\stackrel{”÷}{?}$H2+I2ŹĒæÉÄę·“Ó¦ | |
| C£® | 2H2+O2$\frac{\underline{\;µćČ¼\;}}{\;}$2H2OÓė2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2H2”ü+O2”ü»„ĪŖæÉÄę·“Ó¦ | |
| D£® | Ö»ÓŠæÉÄę·“Ó¦²Å“ęŌŚ»ÆŃ§Ę½ŗā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõČ¼ĮĻµē³ŲµÄøŗ¼«·“Ó¦Ź½£ŗO2+2H2O+4e-ØT4OH- | |
| B£® | øÖĢś·¢Éśµē»ÆѧøÆŹ“µÄÕż¼«·“Ó¦Ź½£ŗFe-2e-ØTFe2+ | |
| C£® | µē½āČŪČŚNaCl£¬Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--2e-=Cl2”ü | |
| D£® | µē½ā±„ŗĶŹ³ŃĪĖ®Ź±£¬Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--2e-=Cl2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÖŅŗ | B£® | ¹żĀĖ | C£® | Õō·¢ | D£® | ¶ą“ĪŃĪĪö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
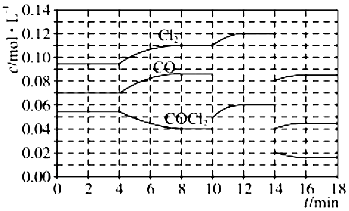 ¹āĘų£ØCOCl2£©ŌŚĖÜĮĻ”¢ÖĘøļ”¢ÖĘŅ©µČ¹¤ŅµÖŠÓŠŠķ¶ąÓĆĶ¾£¬¹¤ŅµÉĻ²ÉÓĆøßĪĀĻĀCOÓėCl2ŌŚ»īŠŌĢæ“ß»ÆĻĀŗĻ³É£®
¹āĘų£ØCOCl2£©ŌŚĖÜĮĻ”¢ÖĘøļ”¢ÖĘŅ©µČ¹¤ŅµÖŠÓŠŠķ¶ąÓĆĶ¾£¬¹¤ŅµÉĻ²ÉÓĆøßĪĀĻĀCOÓėCl2ŌŚ»īŠŌĢæ“ß»ÆĻĀŗĻ³É£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųČÜÓŚĖ®£ŗCl2+H2OØT2H++Cl-+ClO- | |
| B£® | Fe2+ÓėNO3-ŌŚĖįŠŌČÜŅŗÖŠµÄ·“Ó¦£ŗFe2++NO3-+4H+=Fe3++NO”ü+2H2O | |
| C£® | Ļ”ĮņĖįŗĶBa£ØOH£©2ČÜŅŗ·“Ó¦£ŗH++SO42-+Ba2++OH-=BaSO4”ż+H2O | |
| D£® | ÅØĻõĖįÖŠ¼ÓČėĶʬ£ŗCu+4H++2NO3-ØTCu2++2NO2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 50mL3mol/LKClČÜŅŗ | B£® | 75mL2mol/LCaCl2ČÜŅŗ | ||
| C£® | 100mL0.5mol/LBaCl2ČÜŅŗ | D£® | 50mL1mol/LAlCl3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com