
【题目】体积相同、pH也相同的H2SO4溶液和HCl溶液,分别与NaOH溶液中和反应时两者消耗NaOH的物质的量( )
A. 相同 B. H2SO4溶液消耗的NaOH多
C. HCl溶液消耗的NaOH多 D. 无法比较
科目:高中化学 来源: 题型:
【题目】已知1~18号元素的离子![]() 都具有相同的电子层结构,则下列叙述或表示方法正确的是
都具有相同的电子层结构,则下列叙述或表示方法正确的是
A. 四种元素位于同一周期
B. 氢化物的稳定性H2Y>HZ
C. 离子的氧化性![]()
D. a+3<c-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,说明金刚石和石墨是同素异形体的是
A.它们都是熔、沸点很高的晶体
B.它们都是不溶于水的单质
C.二者是不同的单质,在一定条件下能相互转化
D.二者的结构不同,但化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka=1.75×10﹣5 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1=__.
(2)在相同条件下,试比较H2CO3、HCO3﹣和HSO3﹣的酸性强弱:__>__>__.
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液pH随水量的变化图象中:
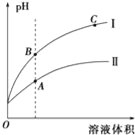
①曲线I表示的酸是__(填化学式).
②A、B、C三点中,水的电离程度最大的是__(填字母).
(4)下列事实不能说明醋酸是弱酸的是_______
①当温度低于16.6℃时醋酸可凝结成冰一样晶体
②0.1mol/L的醋酸钠溶液的pH约为9
③等体积等物质的量浓度的硫酸比醋酸消耗氢氧化钠多
④0.1mol/L的醋酸的pH约为4.8
⑤pH都等于4且等体积的醋酸和盐酸,与等浓度NaOH溶液充分反应时,醋酸消耗碱液多
⑥同物质的量浓度的醋酸和盐酸加水稀释至pH相同时,醋酸加入的水多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气有下列反应:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
(1)该反应中氧化剂是_____;被还原的元素是_______;氧化产物是 ______;
(2)用单线桥法标出电子转移的方向和数目______________;
(3)若该反应中有0.2mol的电子转移,则能生成标准状况下的氯气的体积是_______;
(4)若该反应有1molKMnO4参加反应,被氧化的HCl为______mol,转移电子数______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2H2 (g) +CO (g) ![]() CH3OH (g)达到平衡。下列说法正确的是
CH3OH (g)达到平衡。下列说法正确的是
容器 | 温度/K | 物质的起始浓度/mol.L-l | 物质的平衡浓度/mol.L-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | |
III | 500 | 0 | 0 | 0.10 | 0.025 |
A. 该反应的逆反应放热
B. 达到平衡时,容器I中反应物转化率比容器II中的大
C. 达到平衡时,容器II中c(H2)大于容器III中c(H2)的两倍
D. 达到平衡时,容器III中的正反应速率比容器I中的大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com