
�������ƣ�NaH2PO2�������ڻ�ѧ������
��1����ѧ��������Һ�к���Ni2+ ��H2PO2���������������·������¶�����Ӧ��
�� Ni2+ + H2PO2��+ �� Ni + H2PO3��+
�� 6H2PO2- +2H+ ��2P+4H2PO3-+3H2��
����ƽ��Ӧʽ�١�
��2����Ӧʽ���л�ԭ���� ������ԭԪ���� ��
��3����Ӧ���У�������1 mol H2PO3-����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ mol��
��4���Ӷ�����Ӧ������������1mol Ni��1mol P��ͬʱ�� mol H2PO3�����ɡ�
��5��������и�С���еĻ�ѧ��Ӧ����ʽ��
�������O2��Ӧ����������ϸ��ӣ�����ͨ�������K2O�����������K2O2�����г�������ͳ�������ȡ�Ҫ�Ʊ����������ͨ������һ�����ü������ԭ��Ӧ�Ĺ�����������λ��������Ρ�д�����л�ѧ��Ӧʽ��
������������Ʒ�Ӧ
�ڼػ�ԭ����أ�ͬʱ��������һ�ֵ�������
��1��Ni2++H2PO2+H2O=Ni+H2PO3+2H+ ��2�� H2PO2 Ni ��3��2mol ��4��3 ��5����2Na+Na2O2= 2Na2O
��10K+2KNO3=6K2O+N2
��������
����������۲췴Ӧʽ1��֪����+2�۱��0�ۣ����ϼ۽���2��H2PO2���е�PΪ+1�۱�ΪH2PO3���е�P+3�ۣ����ϼ�����2���ݵ�ʧ����������ȵ�ԭ��������H2PO2������Ҫ�����κε������پ�ԭ�Ӹ����غ��֪����߷�Ӧ��ֻ�������������ұ�������������ڷ�Ӧ���п϶�����һ����ԭ�ӣ�����Ŀ��˵���÷�Ӧʱ�����������½��У����Է�Ӧ����Ӧ����ˮ�����˷�Ӧ�����Կ��Եó�Ni2++H2PO2+H2O=Ni+H2PO3+2H+
H2PO2�� ��P���ϼ����ߣ��������ԭ������Ni2+���ϼ۽����������������Ա���ԭ��Ԫ������
6H2PO2- +2H+ ��2P+4H2PO3-+3H2�� 6H2PO2-��6��P�Ļ��ϼ���+1���2��0�۵�P��4��+3�۵�4H2PO3�е�P���������4Ħ����H2PO3-����ת����4����2��������1Ħ����H2PO3-����ת�Ƶ����ʵ���Ϊ2Ħ����
Ni2++H2PO2+H2O=Ni+H2PO3+2H+ ��֪����һĦ����Ni��ͬʱ����1Ħ����H2PO3�� 6H2PO2- +2H+ ��2P+4H2PO3-+3H2����֪����1Ħ����P��ͬʱ����2Ħ����H2PO3�������ܹ�����3Ħ��H2PO3��
���Ʊ����������ͨ������һ�����ü������ԭ��Ӧ�Ĺ�����������λ��������Ρ���֪
��2Na+Na2O2= 2Na2O ��10K+2KNO3=6K2O+N2
���㣺���黯ѧʽ����ƽ��������ԭ��Ӧ�����ʵ�������ؼ����֪ʶ


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��ѧ��Ҫ������ѧר�����������������йػ�ѧ������ȷ���� (����)
A��H2O�ĵ���ʽ�� B��������Ϊ14��̼ԭ�ӣ�
B��������Ϊ14��̼ԭ�ӣ�
C��CO2�ı���ģ�ͣ� D��Cl���Ľṹʾ��ͼ��
D��Cl���Ľṹʾ��ͼ��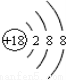
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����߿�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�� ������������ͭ����Һ�ɼ���ʧȥ��ǩ���Ҵ�������������ȩ��������ƿ��ɫ��Һ
B�������������е���Ԫ��ʱ�����Ƚ���������������ữ���ټ���������Һ�����飬ͨ���۲��Ƿ��а�ɫ�������ж��Ƿ������Ԫ��
C�� Ħ�����Ʊ���������мҪ����̼������Һ����ϴ�ӣ�ʹ���ȵ�̼������Һ�������ȥ���۵���������������Һ����ʱ��������������
D�� ���ڱ�������ˮ������Ӧʱ������Ӧ�࣬����ֻ��������ˮ�Ժ����ӵķ�ˮ�����Լ��飬�������������ⶨ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ʢ��NaHSO4��Һ���ձ��в��ϵ�Ba(OH)2��Һ������Ba(OH)2��Һ�IJ��ϵ��룬��Һ�в����ij�������pH�仯�����ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ���ﲻ�ܱ�ʾΪ2-��ϩ����
A��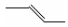 B�� CH3CH��CHCH3 C��
B�� CH3CH��CHCH3 C��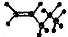 D��
D��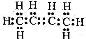
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�����������������������ɵ��γ�Ϊ���Ρ�����CaOCl2��������Һ�п��Է�����Ӧ����Cl2�����й��ڻ���CaOCl2���й��жϲ���ȷ���ǣ�NAΪ�����ӵ�����)
A���û�����������Һ�в���1mol Cl2ʱת�Ƶĵ�����ΪNA
B���û��ε�ˮ��Һ����Ư����
C���û�������Ԫ�صĻ��ϼ�Ϊ+1��-1��
D���û��ξ��н�ǿ�Ļ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A��Ba(OH)2��Һ��ϡ���ᷴӦ��Ba2++OH-+H++SO42-=BaSO4��+H2O
B��Fe��FeCl3��Һ��Ӧ��Fe+Fe3+=2Fe2+
C������ʯ�м���ϡ���CaCO3+2H+=Ca2++CO2��+H2O
D��AlCl3��Һ�мӹ�����ˮ��Al3++3OH-=Al(OH)3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ���� (����)
A�������ױ��ں˴Ź����������ܳ�������壬��������֮��Ϊ3��1
B����ϵͳ�������������� ��������2,2,4,5-�ļ�-3,3-���һ�����
��������2,2,4,5-�ļ�-3,3-���һ�����
C���ṹƬ��Ϊ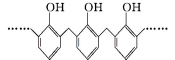 �ĸ߾���䵥���Ǽ�ȩ�ͱ���
�ĸ߾���䵥���Ǽ�ȩ�ͱ���
D������ ��������
��������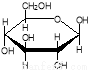 ��Ԫ�������ͬ����ѧʽ��ΪC6H12O6������Cm(H2O)n����ˣ��������������
��Ԫ�������ͬ����ѧʽ��ΪC6H12O6������Cm(H2O)n����ˣ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ̨����·�����߿����ۻ�ѧģ���Ծ����Ծ��������棩 ���ͣ������
CO2�������г����Ļ�����֮һ���������繤ҵ���õķ�չ���˿ڵľ�����ȫ����Դ���ż�������������Խ��Խ���ص����⣬�����CO2�������о����ۺ������������ӡ�
���ڴ��������£����ɼ״���CO2ֱ�Ӻϳ�̼�������(DMC)��CO2 + 2CH3OH �� CO(OCH3)2 + H2O�����״�ת����ͨ�����ᳬ��1%��������Լ�÷�Ӧ����ҵ������Ҫԭ��ij�о�С���������������������£�ͨ���о��¶ȡ���Ӧʱ�䡢���������ֱ��ת����(TON)��Ӱ�������۴����Ĵ�Ч�������㹫ʽΪ��TON��ת���ļ״������ʵ���/���������ʵ�����
��1�����ݷ�Ӧ�¶ȶ�TON��Ӱ��ͼ����ͬʱ���ڲⶨ�����жϸ÷�Ӧ���ʱ��H________0�����������������������������____________________________________��

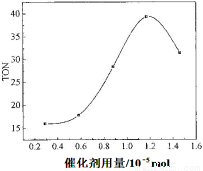
��2�����ݷ�Ӧʱ���TON��Ӱ��ͼ����ͼ������֪��Һ�����10mL����Ӧ��ʼʱ�״�0.25mol������0.6��10��5 mol��������¶��£�4��7 h��DMC��ƽ����Ӧ���ʣ�________��
��3�����ݸ��о�С���ʵ�鼰����������TON��Ӱ��ͼ��������ͼ�����ж�����˵����ȷ���� ��
A���ɼ״���CO2ֱ�Ӻϳ�DMC���������ü״���Ӱ�컷������������CO2 ת��Ϊ��Դ������Դѭ�����úͻ����������涼������Ҫ����
B. �ڷ�Ӧ��ϵ�����Ӻ��ʵ���ˮ��������߸÷�Ӧ��TON
C. ��������������1.2��10��5 molʱ�����Ŵ������������ӣ��״���ƽ��ת�����������
D. ��������������1.2��10��5 molʱ�����Ŵ�������������DMC�IJ��ʷ��������½�
��.��������ڵ�CO2����˳���ų������������ж���������Һ���Ե������������������ҺpH��Ӱ�죬����ѪҺ����Ҫͨ��̼�����λ�����ϵ(H2CO3/HCO3-)ά��pH�ȶ�����֪��������ѪҺ����������ʱ��H2CO3��һ�����볣��Ka1=10-6.1��c(HCO3-):c(H2CO3)��20:1��lg2=0.3��
(4)��������ݿ������������ѪҺ��pH________(����һλС��)��
(5)��������ѪҺ��H2CO3��HCO3-��OH- ��H+������Ũ���ɴ�С��ϵΪ�� ��
(6)���������ᡢ�����ѪҺ��ʱ��ѪҺpH�仯������ԭ���ǡ��������������������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com