
��9�֣������Ѿ����Ƴ��Ա���Ϊȼ�ϵ�����ȼ�ϵ�أ������Ϊ����̼���Σ�����ܷ�Ӧ����ʽΪ��C3H8+5O2=3CO2+4H2O��
��1����֪��2C3H8��g��+7O2��g��=6CO��g��+8H2O��l��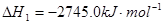
C��s��+O2��g��=CO2��g�� 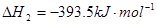
2C��s��+O2��g��=2CO��g�� 
��ӦC3H8��g��+5O2��g��=3CO2��g��+4H2O��1���ġ�H___________________��.
��2���õ�ص�����ͨ��O2��CO2������ͨ����飬�������ĵ缫��ӦʽΪ_________________����ع���ʱCO32������_____________����
��3���øõ�ص��1L 1 mol��L��1��AgNO3��Һ���˵��ط�Ӧ�Ļ�ѧ����ʽΪ______________________�����õ������0.005molC3H8ʱ��������Һ��pHΪ__________����Һ����仯���Բ��ƣ�
��1����2221.5kJ��mol��1��2�֣���λ��λд�������֣�
��2��O2+2CO2+4e�� =2CO32����2�֣�����1�֣�
��3��4AgNO3+2H2O 4Ag+O2�� +4HNO3��2�֣���д��Ӧ��������ƽ�����֣�
4Ag+O2�� +4HNO3��2�֣���д��Ӧ��������ƽ�����֣�
1��2�֣�
���������������1�����ݷ���ʽ�Ⱥ�˳����ֱ�Ϊ�١��ڡ��ۣ�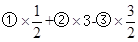 ���õ�����ʽC3H8��g��+5O2��g��=3CO2��g��+4H2O��1������Ӧ��Ҳ������ʽ�����H=
���õ�����ʽC3H8��g��+5O2��g��=3CO2��g��+4H2O��1������Ӧ��Ҳ������ʽ�����H=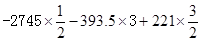 =��2221.5kJ��mol��1��
=��2221.5kJ��mol��1��
��2��������������Ӧ��O2+2CO2+4e��=2CO32����ԭ��������������ƶ���
��3��������������Ƿ��������ͣ�4AgNO3+2H2O 4Ag+O2�� +4HNO3�����õ������0.005molC3H8ʱ��ת�Ƶ�����0.1mol������0.1molH+��������Ũ��Ϊ0.1mol/L��pHΪ1��
4Ag+O2�� +4HNO3�����õ������0.005molC3H8ʱ��ת�Ƶ�����0.1mol������0.1molH+��������Ũ��Ϊ0.1mol/L��pHΪ1��
���㣺�����Ȼ�ѧ����ʽ����д�����㣬ԭ�������ص�ԭ�������㡣
��������˹����Ҫ��ʽ������Ӽ�����Ӧ��Ҳ������Ӽ������ڽ��ۺ��⡣


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ������2012�����12���¿���ѧ���� ���ͣ�022
�����Ѿ����Ƴ��Ա���Ϊȼ�ϵ�����ȼ�ϵ�أ������Ϊ�������Σ�����ܷ�Ӧ����ʽΪ��C3H8��5O2![]() 3CO2��4H2O��
3CO2��4H2O��
(1)��֪��2C3H8(g)��7O2(g)![]() 6CO(g)��8H2O(l)��H1����2745.0 kJ��mol��1
6CO(g)��8H2O(l)��H1����2745.0 kJ��mol��1
C(s)��O2(g)![]() CO2(g)��H2����393.5 kJ��mol��1
CO2(g)��H2����393.5 kJ��mol��1
2C(s)��O2(g)![]() 2CO(g)��H3����221.0 kJ��mol��1
2CO(g)��H3����221.0 kJ��mol��1
��ӦC3H8(g)��5O2(g)![]() 3CO2(g)��4H2O(l)�Ħ�H________��
3CO2(g)��4H2O(l)�Ħ�H________��
(2)�õ�ص�����ͨ��O2��CO2������ͨ����飬�������ĵ缫��ӦʽΪ________����ع���ʱCO32������________����
(3)�øõ�ص��1 L��1 mol��L��1��AgNO3��Һ���˵��ط�Ӧ�Ļ�ѧ����ʽΪ________�����õ������0.005 mol��C3H8ʱ��������Һ��pHΪ________(��Һ����仯���Բ���)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ������Ծ��ѧ����12���¿���ѧ�Ծ��������棩 ���ͣ������
��9�֣������Ѿ����Ƴ��Ա���Ϊȼ�ϵ�����ȼ�ϵ�أ������Ϊ����̼���Σ�����ܷ�Ӧ����ʽΪ��C3H8+5O2=3CO2+4H2O��
��1����֪��2C3H8��g��+7O2��g��=6CO��g��+8H2O��l��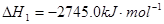
C��s��+O2��g��=CO2��g�� 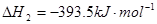
2C��s��+O2��g��=2CO��g�� 
��ӦC3H8��g��+5O2��g��=3CO2��g��+4H2O��1���ġ�H___________________��.
��2���õ�ص�����ͨ��O2��CO2������ͨ����飬�������ĵ缫��ӦʽΪ_________________����ع���ʱCO32������_____________����
��3���øõ�ص��1L 1 mol��L��1��AgNO3��Һ���˵��ط�Ӧ�Ļ�ѧ����ʽΪ______________________�����õ������0.005molC3H8ʱ��������Һ��pHΪ__________����Һ����仯���Բ��ƣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ɽ��ʡ�����и���12���¿���ѧ�Ծ� ���ͣ������
��9�֣������Ѿ����Ƴ��Ա���Ϊȼ�ϵ�����ȼ�ϵ�أ������Ϊ�������Σ����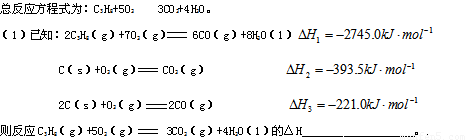
��2���õ�ص�����ͨ��O2��CO2������ͨ����飬�������ĵ缫��ӦʽΪ__________________________________����ع���ʱCO32������_____________����
��3���øõ�ص��1L 1 mol��L��1��AgNO3��Һ���˵��ط�Ӧ�Ļ�ѧ����ʽΪ_________________________________________________�����õ������0.005molC3H8ʱ��������Һ��pHΪ__________����Һ����仯���Բ��ƣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com