

| ||
| ||


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����¶��£�0.31 mol?L-1 HF��Һ��pH=2 |
| B�������¶Ȼ�����Ũ�ȣ�HF�ĵ���ƽ�ⳣ���������� |
| C������Һ��Ϻ�������� |
| D���͵�CaF2��Һ�м�ˮ��c��Ca2+��һ���ȼ�ˮǰС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
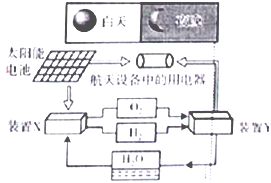 ��ͼ��һ�ֺ�������������ϵͳԭ��ʾ��ͼ������˵����ȷ����
��ͼ��һ�ֺ�������������ϵͳԭ��ʾ��ͼ������˵����ȷ����| A����ϵͳ��ֻ����3����ʽ������ת�� |
| B��װ��Y�и����ĵ缫��ӦʽΪ��O2+2H2O+4e-=4OH- |
| C��װ��X��ʵ��ȼ�ϵ�ص�ȼ�Ϻ����������� |
| D����ϵͳ��ʵ�����ʵ����ŷţ�����ʵ�ֻ�ѧ������ܼ����ȫת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 100�� | 300�� | 500�� |
| K | 0.125 | 0.95 | 3.2 |
| c(CO2)?[c(N2)]2 |
| c(N2O)2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ�������
��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ�������| A��5.4gˮ�к���ԭ����Ϊ0.3NA |
| B��25�棬1L pH=12�İ�ˮ�У�����OH-����ĿΪ0.1 NA |
| C����״���£�32g�ṹ��ͼ����S-S����ĿΪNA |
| D���ڷ�ӦKIO3+6HI=3I2+KI+3H2O�У�ÿ����l mol I2ת�Ƶ�����Ϊ2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������ܲ�����������Һ�У�NH4+��Fe2+��SO42-��NO3- |
| B����ɫ������Һ�У�Ba2+��H+��MnO4-��Br- |
| C��ʹ���ȱ�����Һ�У�NH4+��NO3-��Na+��SO42- |
| D����ʹ���۵⻯����ֽ����ɫ����Һ�У�K+��SO42-��S2-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��Fe2+��Cr2O72-��SO42- |
| B��Al3+��Na+��SO42-��HCO3- |
| C��Na+��Cu2+��Cl-��S2- |
| D��Fe3+��K+��SCN-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��FeI��Һ�в���ͨ��Cl2����Һ��I-��Cl-��I
��FeI��Һ�в���ͨ��Cl2����Һ��I-��Cl-��I| O | - 3 |
| O | - 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com