
| A. | 向硫酸铝溶液中滴加过量的氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 金属铜与浓硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 实验室制备氢氧化铁胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ | |
| D. | 向苯酚钠溶液中通入少量的二氧化碳气体:2C6H5ONa+CO2+H2O═2C6H6O+Na2CO3 |
分析 A.一水合氨是弱碱,应该写化学式,且生成的氢氧化铝不溶于氨水;
B.铜和稀硝酸反应生成硝酸铜、NO和水,和浓硝酸反应生成二氧化氮;
C.在沸水中氯化铁水解生成氢氧化铁胶体,应该写可逆号;
D.苯酚钠和二氧化碳、水反应生成碳酸氢钠和苯酚.
解答 解:A.一水合氨是弱碱,应该写化学式,且生成的氢氧化铝不溶于氨水,离子方程式为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故A错误;
B.铜和稀硝酸反应生成硝酸铜、NO和水,和稀硝酸反应离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,和浓硝酸反应离子方程式为Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故B错误;
C.在沸水中氯化铁水解生成氢氧化铁胶体,离子方程式为Fe3++3H2O═Fe(OH)3(胶体)+3H+,故C正确;
D.苯酚钠和二氧化碳、水反应生成碳酸氢钠和苯酚,化学方程式为C6H5ONa+CO2+H2O═C6H6O+NaHCO3,故D错误;
故选C.
点评 本题考查离子方程式或化学方程式的书写,明确物质的性质及反应实质是解本题关键,注意氢氧化铝不溶于弱碱但能溶于强碱,易错选项是D,无论二氧化碳是否过量都生成碳酸氢钠,为易错点.


科目:高中化学 来源: 题型:选择题
| 物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
| Ksp(单位略) | 1.1×10-11 | 2.3×10-3 | 1.8×10-10 | 1.9×10-12 |
| A. | 浓度均为0.2 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 | |
| B. | 将O.001 mol•L-1的AgN03溶液滴入O.001 mol•L-1的KCl和O.001 mol•L-1 的K2CrO4混合溶液中.先产生Ag2Cr04沉淀 | |
| C. | 0.ll mol•L-1的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 | |
| D. | 在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极.该电池的电解质为6mol/LKOH溶液,下列说法正确的是( )
一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极.该电池的电解质为6mol/LKOH溶液,下列说法正确的是( )| A. | 放电时镍电极反应为:NiO(OH)+H2O+e-=Ni(OH)2+OH- | |
| B. | 放电时OH-移向镍电极 | |
| C. | 充电时碳电极反应为H2-2e-+2OH-=2H2O | |
| D. | 充电时将碳电极与电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | C一O | Si-Si | Si-H | Si一O |
| 键能/(kJ•mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
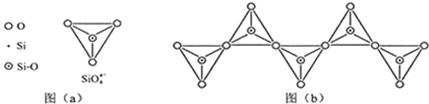
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 将pH=1的醋酸和pH=13的NaOH溶液等体积混合后的溶液c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| C. | 等体积等物质的量浓度的NaCl和CH3COONa两种溶液中离子总数:前者小于后者 | |
| D. | 等体积等物质的量浓度的HCl溶液和CH3COONa溶液混合后:c(CH3COOH)+c(CH3COO-)═c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的盐酸溶液中含有的阳离子数为0.02NA | |
| B. | 1mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| C. | 标准状况下,22.4L CHCl3所含有的分子数目为NA | |
| D. | 27g铝与足量的盐酸或NaOH溶液反应转移的电子数目均为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a、c两元素处在元素周期表的VIA族 | |
| B. | b、d两种元素可组成化学式为d2b2的化合物,且阴阳离子个数比为1:2 | |
| C. | c单质可在b单质中燃烧生成的化合物的分子式为cb2 | |
| D. | c的单质可用来制作光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2,且均能与水反应 | |
| B. | 根据非金属性强弱,不可能由Z的最高价氧化物制出W的最高价氧化物 | |
| C. | Y的简单氢化物的沸点和热稳定性均大于R的简单氢化物 | |
| D. | 向两份BaCl2溶液中分别通入RY2、WY2,均无白色沉淀生成,但一段时间后,通入RY2的一份中可能产生沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com