
分析 ①当x=1.3时,即KxFeO2为K1.3FeO2,其最简整数比的化学式为K13Fe10O20,即$\frac{13}{2}$K2O•3FeO•$\frac{7}{2}$Fe2O3;
②当x=1.4时,即K1.4FeO2,当其在稀硫酸条件下与足量的KI溶液反应时,其反应实质是Fe3+和I-在酸性条件下发生氧化还原反应生成Fe2+和I2,K1.4FeO2的化学组成可看作7K2O•4FeO•3Fe2O3,结合电子守恒、原子守恒书写反应方程式.
解答 解:①当x=1.3时,即KxFeO2为K1.3FeO2,其最简整数比的化学式为K13Fe10O20,即$\frac{13}{2}$K2O•3FeO•$\frac{7}{2}$Fe2O3,则a:b:c=$\frac{13}{2}$:3:$\frac{7}{2}$=13:6:7,
故答案为:13:6:7;
②当x=1.4时,即K1.4FeO2,当其在稀硫酸条件下与足量的KI溶液反应时,其反应实质是Fe3+和I-在酸性条件下发生氧化还原反应生成Fe2+和I2,K1.4FeO2的化学组成可看作7K2O•4FeO•3Fe2O3,由电子、原子守恒可知反应的方程式为10K1.4FeO2+6KI+20H2SO4=10FeSO4+3I2+10K2SO4+20H2O,
故答案为:10K1.4FeO2+6KI+20H2SO4=10FeSO4+3I2+10K2SO4+20H2O.
点评 本题考查物质组成的计算及氧化还原反应,为高频考点,把握物质中的定组成、氧化还原反应的应用为解答的关键,侧重分析与应用能力的考查,注意守恒法应用,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.04 mol/(L•s) | B. | 0.12 mol/(L•s) | C. | 0.4 mol/(L•s) | D. | 1.2 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿 | |
| B. | 汽车尾气排放的NO2等气体是造成光化学污染的主要原因 | |
| C. | 点燃爆竹后,硫燃烧生成SO3 | |
| D. | 误食含有大量Cu2+的食物可以服用鲜牛奶解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质都是离子化合物,因此NaCl是离子化合物 | |
| B. | 亚硫酸溶液的导电能力可能比稀硫酸强 | |
| C. | SO3溶于水,其水溶液能导电,SO3是电解质 | |
| D. | 石墨是单质,能导电,因此石墨是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键 | |
| B. | 常温呈气态的单质分子中均存在共价键 | |
| C. | 含有极性键的分子一定是极性分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
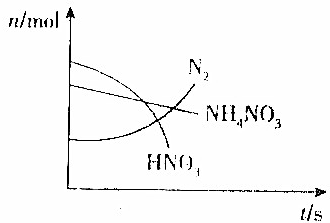 某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )| A. | N2是还原产物,Zn(NO3)2是氧化产物 | |
| B. | NH4NO3是氧化剂,Zn是还原剂 | |
| C. | 反应生成1molN2时共有5mol电子转移 | |
| D. | HNO3在反应中没有表现出酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| B. | 标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数等于2NA | |
| C. | NO2和H2O反应每生成2 mol HNO3时转移的电子数目为2NA | |
| D. | 1 mol Fe在氧气中充分燃烧失去3NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com