
| A、电解精炼铜时,转移1mol电子,阳极上溶解的铜原子数必为0.5NA | ||||
| B、常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3×6.02×1023 | ||||
| C、等体积0.2mol?L-1HCl溶液与0.05mol?L-1Ba(OH)2溶液混合后,溶液的pH=1 | ||||
D、溶液中由水电离出的c(H+)=1×10-12mol?L-1,S
|


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:
| A、60g SiO2中含有NA个SiO2分子 | B、标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA | C、1mol CO2与含1mol NaOH的溶液反应后,溶液中HCO3-数为NA | D、1mol C5H12分子中共价键总数为16NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,5.6 L一氧化氮和5.6 L氧气混合,混合物分子总数为0.5NA | B、标准状况下,11.2L氨气溶于水配制成500mL溶液,溶液中NH4+数目为1.0NA | C、在Zn+2H3NO+NH4NO3=Zn(NO3)2+N2↑+3H2O反应中,若生成14.0gN2,则转移电子数为NA | D、标准状况下,含NA个分子的CO、C2H4混合气体,其质量为28g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol羟基(-OH)所含的电子数约为10NA | B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0NA | C、25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA | D、53.5gNH4Cl中含有H-Cl键的个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,46gN02与N204的混合气体中含有的原子数为3NA | B、15.6 g Na2O2与过量CO2反应时,转移的电子数为O.4NA | C、常温常压下,11.2L 二氧化硫中所含的氧原子数等于NA | D、1L 1 mol?L-1 的Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,5.6L CCl4含有的C-Cl共价键数为NA | B、2.4g Mg与足量稀硫酸反应时,失去电子数为0.1NA | C、l L0.5mol.L-1 CuCl2 溶液中含有的 Cu2+数为0.5NA | D、16g氧气和臭氧的混合物中氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,18g H218O中含有的原子数小于3NA | B、标准状况下,22.4L HF中含有的氟原子数目为NA | C、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | D、4.6g Na与O2反应生成Na2O和Na2O2,转移电子数介于0.1NA~0.2NA之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁与足量稀硝酸反应,1mol Fe失去电子数为3NA | B、常温常压下,22.4L乙烯中含极性共价键数目为3NA | C、1L 1mol?L-1的NH4Cl溶液中有NA个NH4+ | D、1mol冰醋酸和lmol乙醇在浓硫酸加热下充分反应生成H2O个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
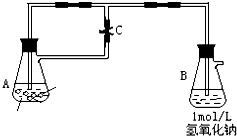 图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:
图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com