
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

分析 (1)反应在55℃条件下进行,需要水浴加热,且有冷凝回流装置;可用葡萄糖氧化酶催化作用下用氧气氧化葡萄糖,可生成葡萄糖酸;
(2)CaCO3固体需有剩余,可使葡萄糖酸完全反应,氯化钙易溶于水,易引入杂质,且葡萄糖酸与氯化钙不反应;
(3)趁热过滤,可避免葡萄糖酸钙的损失;
(4)由表中数据可知,葡萄糖酸钙微溶于乙醇,可避免损失;
(5)洗涤沉淀,应避免沉淀溶解,且能将沉淀吸附物冲洗去.
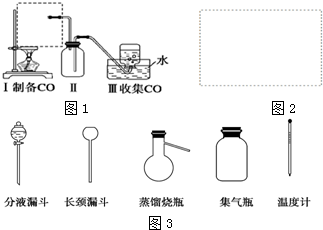
解答 解:(1)反应在55℃条件下进行,需要水浴加热,且有冷凝回流装置,题中A缺少回流装置,要滴加溴水,所以要有滴液漏斗,排除A,C缺少水浴加热,只有B符合;新制Cu(OH)2悬浊液、[Ag(NH3)2]OH溶液氧化性较弱,且反应需要碱性条件下进行,不利于葡萄糖的氧化,而酸性高锰酸钾氧化性较强,不能得到葡萄糖酸,可用葡萄糖氧化酶催化作用下用氧气氧化葡萄糖,可生成葡萄糖酸,
故答案为:B;AD;
(2)可使葡萄糖酸完全转化为葡萄糖酸钙,使葡萄糖酸、HBr完全转化为钙盐,则加入的碳酸钙应过量,因盐酸酸性比葡萄糖酸强,则加入氯化钙与葡萄糖酸、HBr难以反应,且易引入杂质,不易分离,应用碳酸钙,
故答案为:使葡萄糖酸、HBr完全转化为钙盐;葡萄糖酸、HBr与 CaCl2不反应;
(3)温度高时,葡萄糖酸钙的溶解度较大,趁热过滤,可避免葡萄糖酸钙的损失,
故答案为:葡萄糖酸钙冷却后结晶析出,如不趁热过滤会损失产品;
(4)由表中数据可知,葡萄糖酸钙微溶于乙醇,用乙醇洗涤可避免损失,有利于葡萄糖酸钙析出,
故答案为:可降低葡萄糖酸钙在溶剂中的溶解度,有利于葡萄糖酸钙析出;
(5)洗涤沉淀,应避免沉淀溶解,且能将沉淀吸附物冲洗去,可用乙醇-水混合溶液,如只用水,则造成葡萄糖酸钙溶解而损失,只用乙醇,不能将杂质全被洗去,
故答案为:C.
点评 本题为2014年浙江考题,侧重于物质的制备、分离和提纯的考查,着重于学生的分析能力和实验能力的考查,由于培养学生的良好的科学素养,难度中等.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其它条件不变,使用不同催化剂,该反应的平衡常数不变 | |
| B. | 平衡前,随着反应的进行,容器内压强始终不变 | |
| C. | 平衡时,其它条件不变,分离出少量的硫,正反应速率不变 | |
| D. | 平衡时,其他条件不变,升高温度可使反应速率加快,平衡常数减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com