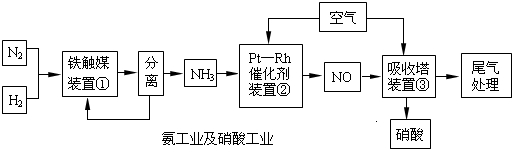
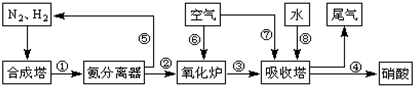
工业合成氨与制备硝酸一般可连续生产,流程如下:
Ⅰ.合成氨
(1)写出装置①中发生反应(该反应为放热反应)的化学方程式:______________
(2)进入装置①的氮、氢混合气体(体积比为1:3)与反应达平衡后出来的混合气体压强之比为5:4,则氮气的转化率为______________。
(3)生产过程中氮气与氢气以1:2.8(体积比)进行投料,试从原料利用的角度解释原因_______________________
(4)已知在实际生产过程中装置①中温度控制在700K左右,这样做的目的是:
①该温度下铁触媒的活性最大,催化效果最佳;
②____________________
Ⅱ.氨的接触氧化原理
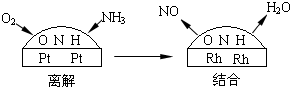
(5)在装置②中反应有:
4NH
3(g) + 5O
2(g)

4NO(g)+ 6H
2O(g);ΔH=—905.5 kJ·mol
-1 4NH
3(g) + 3O
2(g)

2N
2(g) + 6H
2O(g);ΔH=—1267 kJ·mol
-1 除了上列反应外还可能发生一氧化氮的分解。完成热化学方程式:
2NO(g)

N
2(g) +O
2(g);ΔH=__________
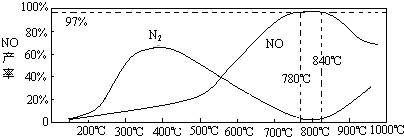
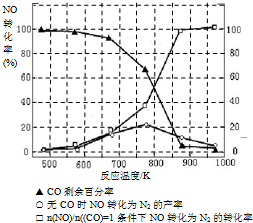
(6)根据下图信息回答问题
装置②中将温度控制在780℃-840℃,不可超过900℃,其原因是____________________


 4NO(g)+ 6H2O(g);ΔH=—905.5 kJ·mol-1
4NO(g)+ 6H2O(g);ΔH=—905.5 kJ·mol-1  2N2(g) + 6H2O(g);ΔH=—1267 kJ·mol-1
2N2(g) + 6H2O(g);ΔH=—1267 kJ·mol-1  N2(g) +O2(g);ΔH=__________
N2(g) +O2(g);ΔH=__________
 步步高达标卷系列答案
步步高达标卷系列答案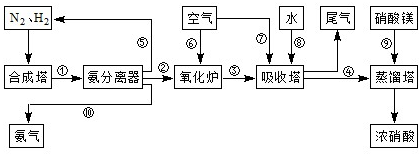
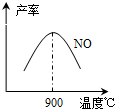 (3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因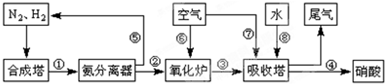
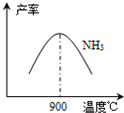 (3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示.温度高于900℃时,NH3产率下降的原因
(3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示.温度高于900℃时,NH3产率下降的原因