
| ���ữѧʽ | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� | 1.8��10-5 | 4.9��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
| A�� | 1mol/L������Һ��ˮϡ�ͺ���������Ũ�Ⱦ���С | |
| B�� | Na2CO3��Һ�У�һ����2c��Na+��=c��H2CO3��+c��HCO3-��+c��CO32-�� | |
| C�� | �����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��Na2CO3����pH��NaCN����pH��CH3COONa�� | |
| D�� | 1 mol•L-1HCN��Һ��1mol•L-1NaOH��Һ�������Ϻ��������Һ������ |
���� A����ˮϡ�ʹٽ�������룬�������������̶�С����Һ�������̶ȵ�����Һ��c��H+����С���¶Ȳ��䣬ˮ�����ӻ��������䣬�ݴ��ж���Һ��c��OH-���仯��
B���κε������Һ�ж����������غ㣬���������غ��жϣ�
C����ĵ���ƽ�ⳣ��Խ����ĵ���̶�Խ�����������Խǿ�����ݱ�������֪���������ǿ��˳����CH3COOH��H2CO3��HCN��HCO3-����ĵ���̶�Խ�������Ӧ���������ˮ��̶�ԽС������ͬŨ�ȵ�������Һ��pHԽС��
D.1 mol•L-1HCN��Һ��1mol•L-1NaOH��Һ�������Ϻ�ǡ�÷�Ӧ����NaCN��NaCNΪǿ�������Σ�����Һ�ʼ��ԣ�
��� �⣺A����ˮϡ�ʹٽ�������룬�������������̶�С����Һ�������̶ȵ�����Һ��c��H+����С���¶Ȳ��䣬ˮ�����ӻ��������䣬����Һ��c��OH-������A����
B���κε������Һ�ж����������غ㣬���������غ��c��Na+��=2[c��H2CO3��+c��HCO3-��+c��CO32-��]����B����
C����ĵ���ƽ�ⳣ��Խ����ĵ���̶�Խ�����������Խǿ�����ݱ�������֪���������ǿ��˳����CH3COOH��H2CO3��HCN��HCO3-����ĵ���̶�Խ�������Ӧ���������ˮ��̶�ԽС������ͬŨ�ȵ�������Һ��pHԽС���������ˮ��̶�CO32-��CN-��CH3COO-�����Ե����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��Na2CO3����pH��NaCN����pH��CH3COONa������C��ȷ��
D.1 mol•L-1HCN��Һ��1mol•L-1NaOH��Һ�������Ϻ�ǡ�÷�Ӧ����NaCN��NaCNΪǿ�������Σ����������ˮ�������Һ�ʼ��ԣ���D����
��ѡC��
���� ���⿼������Ũ�ȴ�С�Ƚϣ�Ϊ��Ƶ���㣬��ȷ�������ƽ�ⳣ�����������ˮ��̶ȹ�ϵ�ǽⱾ��ؼ����״�ѡ����C��ע��CO32-��Ӧ������HCO3-������H2CO3��Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 55 kJ | B�� | 220 kJ | C�� | 550 kJ | D�� | 1 108 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50mL 3mol/L KCl��Һ | B�� | 75 mL 2mol/L CaCl2��Һ | ||
| C�� | 100 mL 0.5mol/L BaCl2��Һ | D�� | 50mL 1mol/L AlCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ����ɫ��dz��ɫ��˵����ˮ�к���Cl2 | |
| B�� | ����ˮ�еμ������ữ��AgNO3��Һ��������ɫ������˵����ˮ�к���Cl- | |
| C�� | ����ˮ�м���NaHCO3��ĩ�������ݲ�����˵����ˮ�к���H+ | |
| D�� | ��FeCl2��Һ�еμ���ˮ����Һ��ɫ����ػ�ɫ��˵����ˮ�к���HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ۢܢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������ʹ�õĹ����β��� | |
| B�� | �����ڼ����ۻ�ʱ�й̶����۵� | |
| C�� | ����ͨ��������Ҫԭ���Ǵ��ʯ��ʯ��ʯӢ | |
| D�� | ��ͨˮ��ijɷ���Ҫ�ǹ����ơ�����ƺͶ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢܢݢ� | B�� | �ڢۢ٢ܢ� | C�� | �٢ڢۢܢ� | D�� | �ڢ٢ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
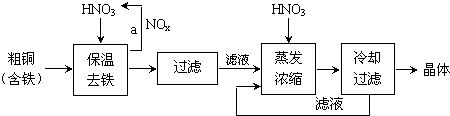
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com