
£Ø»ÆѧÓė¼¼Źõ£©Ä³»Æ¹¤³§ĪŖĮĖ×ŪŗĻĄūÓĆÉś²ś¹ż³ĢÖŠµÄø±²śĘ·CaSO4£¬ÓėĻąĮŚµÄŗĻ³É°±³§ĮŖŗĻÉč¼ĘĮĖŅŌĻĀÖʱø(NH4)2SO4µÄ¹¤ŅÕĮ÷³Ģ£ŗ
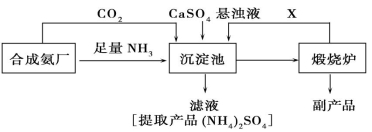
Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©ŗĻ³É°±·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ £¬øĆ·“Ó¦ŌŚ £ØĢīÉč±øĆū£©ÖŠ·¢Éś”£³Įµķ³ŲÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦·½³ĢŹ½ŹĒ £¬øĆ·“Ó¦Äܹ»·¢ÉśµÄŌŅņŹĒ ”£
£Ø2£©ŌŚÉĻŹöĮ÷³ĢµÄ³Įµķ³ŲÖŠĶØČė×ćĮæ°±ĘųµÄÄæµÄŹĒ £¬æÉŅŌŃ»·Ź¹ÓƵÄXŹĒ ”£
£Ø3£©øĆÉś²ś¹ż³ĢÖŠµÄø±²śĘ·ŹĒ ”£“ÓĀĢÉ«»ÆѧŗĶ׏Ō“×ŪŗĻĄūÓĆµÄ½Ē¶ČĖµĆ÷ÉĻŹöĮ÷³ĢµÄÖ÷ŅŖÓŵćŹĒ ”£
 ½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗŚĮś½Ź”ø߶žÉĻæŖѧ²ā»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijŠ©»ÆѧÖŖŹ¶ÓĆŹżÖį±ķŹ¾ÄÜĢåĻÖ³öŠĪĻóÖ±¹Ū”¢¼ņĆ÷Ņ×¼ĒµÄĢŲµć”£ĻĀĮŠÓĆŹżÖį±ķŹ¾²»ŗĻĄķµÄŹĒ
A£®Cl2ÓėCCl4Č”“ś·“Ó¦ŗóµÄ²śĪļ |
|
B£®ĻņÉÕ¼īŅŗÖŠĶØČėSO2ŗóµÄ²śĪļ |
|
C£®ĢśŗĶĻ”ĻõĖį·“Ó¦ |
|
D£®ĻņAlCl3ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£¬ĀĮŌŖĖŲµÄ“ęŌŚŠĪŹ½ |
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓ±±Ź”øßŅ»ÉĻ9.4ÖÜæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶žŃõ»Æ¹čµÄ»ÆѧŠŌÖŹŗܲ»»īĘĆ£¬¼øŗõĖłÓŠµÄĖį¶¼²»ÓėĘä·“Ó¦£¬µ«ÓŠŅ»ÖÖĖįÄܹ»ŗĶ¶žŃõ»Æ¹č·¢Éś·“Ó¦£¬ÕāÖÖĖįŹĒ£Ø £©
A£®ÅØŃĪĖį B£®ĮņĖį C£®ĻõĖį D£®Ēā·śĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚČż“ĪÖÜĮ·»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ijÖÖļ®Ąė×Óµē³ŲµÄÕż¼«²ÄĮĻŹĒ½«ŗ¬ÓŠīÜĖįļ®(LiCoO2)µÄÕż¼«·Ū¾łŌČĶæø²ŌŚĀĮ²ÉĻÖĘ³ÉµÄ£¬æÉŅŌŌŁĄūÓĆ”£Ä³Š£ŃŠ¾æŠ”×é³¢ŹŌ»ŲŹÕ·Ļ¾ÉÕż¼«²ÄĮĻÖŠµÄīÜ”£

£Ø1£©īÜĖįļ®(LiCoO2)øÄŠ“ĪŖŃõ»ÆĪļŠĪŹ½ĪŖ ”£
£Ø2£©25”ꏱ£¬ÓĆĶ¼1ĖłŹ¾×°ÖĆ½ųŠŠµē½ā£¬ÓŠŅ»¶ØĮæµÄīÜŅŌCo2+µÄŠĪŹ½“ÓÕż¼«·ŪÖŠ½ž³ö£¬ĒŅĮ½¼«¾łÓŠĘųÅŻ²śÉś£¬Ņ»¶ĪŹ±¼äŗóÕż¼«·ŪÓėĀĮ²°žĄė”£
¢ŁŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗLiCoO2+4H++e-=Li++Co2++2H2O”¢ ”£Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
¢ŚøĆŃŠ¾æŠ”×é·¢ĻÖĮņĖįÅØ¶Č¶ŌīܵĽž³öĀŹÓŠ½Ļ“óÓ°Ļģ£¬Ņ»¶ØĢõ¼žĻĀ£¬²āµĆĘä±ä»ÆĒśĻßČēĶ¼2ĖłŹ¾”£µ±c(H2SO4)>0.4mol”¤L-1Ź±£¬īܵĽž³öĀŹĻĀ½µ£¬ĘäŌŅņæÉÄÜĪŖ ”£
£Ø2£©µē½āĶź³ÉŗóµĆµ½ŗ¬Co2+µÄ½ž³öŅŗ£¬ĒŅÓŠÉŁĮæÕż¼«·Ū³Į»żŌŚµē½ā²Ūµ×²æ”£ÓĆŅŌĻĀ²½Öč¼ĢŠų»ŲŹÕīÜ”£
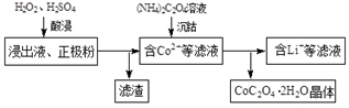
¢ŁŠ“³ö”°Ėį½ž”±¹ż³ĢÖŠÕż¼«·Ū·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£øĆ¹ż³ĢÖŠŅ²æÉŅŌÓĆNa2S2O3“śĢęH2O2£¬Ōņ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
¢ŚŅŃÖŖ(NH4)2C2O4ČÜŅŗ³ŹČõĖįŠŌ£¬ĻĀĮŠ¹ŲĻµÖŠÕżČ·µÄŹĒ (Ģī×ÖÄøŠņŗÅ)”£
A£®c(NH4+)>c(C2O42-)>c(H+)>c(OH-)
B£®c(H+)+c(NH4+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C£®c(NH4+)+c(NH3•H2O )=2[c(C2O42-)+c(HC2O4-)+c(H2C2O4)]
£Ø4£©ŅŃÖŖĖłÓĆļ®Ąė×Óµē³ŲµÄÕż¼«²ÄĮĻĪŖxg£¬ĘäÖŠLiCoO2(M=98g”¤mol-1)µÄÖŹĮæ·ÖŹżĪŖa%£¬Ōņ»ŲŹÕŗóµĆµ½CoC2O4•2H2O(M=183g”¤mol-1)µÄÖŹĮæ²»øßÓŚ g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚČż“ĪÖÜĮ·»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
0.1mol½šŹōĪżøś100mL12mol/LHNO3¹²ČČŅ»¶ĪŹ±¼ä£¬ĶźČ«·“Ó¦ŗó·Å³öĘųĢå0.4mol,²ā¶ØČÜŅŗc(H+)=8mol/L£¬ČÜŅŗĢå»żČŌĪŖ100mL”£ÓÉ“ĖĶʶĻŃõ»Æ²śĪļæÉÄÜŹĒ
A£®Sn(NO3)2 B£®Sn(NO3)4
C£®SnO2•4H2O D£®Sn(NO3)2ŗĶSn(NO3)4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ¹óÖŻŹ”øßČżŅ»Ä£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ŌČżĮŖ±½ŹĒŅ»ÖÖÓŠ»śŗĻ³ÉµÄÖŠ¼äĢ唣¹¤ŅµÉĻŗĻ³É¶ŌČżĮŖ±½µÄ»Æѧ·½³ĢŹ½ĪŖ
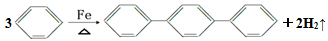
ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ( )
A. ÉĻŹö·“Ó¦ŹōÓŚČ”“ś·“Ó¦
B. ¶ŌČżĮŖ±½µÄŅ»ĀČČ”“śĪļÓŠ3ÖÖ
C. 1 mol¶ŌČżĮŖ±½ŌŚ×ćĮæµÄŃõĘųÖŠĶźČ«Č¼ÉÕĻūŗÄ21.5 mol O2
D. ¶ŌČżĮŖ±½·Ö×ÓÖŠÖĮÉŁÓŠ16øöŌ×Ó¹²Ę½Ćę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗžÄĻŹ”ø߶žÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻĀ±ķŹĒA”¢B”¢C”¢D”¢EĪåÖÖÓŠ»śĪļµÄÓŠ¹ŲŠÅĻ¢£ŗ

øł¾Ż±ķÖŠŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AÓėäåĖ®·“Ó¦µÄÉś³ÉĪļµÄĆū³Ę½Š×ö £»Š“³öŌŚŅ»¶ØĢõ¼žĻĀ£¬AÉś³Éøß·Ö×Ó»ÆŗĻĪļµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø2£©AÓėĒāĘų·¢Éś¼Ó³É·“Ó¦ŗóÉś³É·Ö×ÓF£¬ÓėFŌŚ·Ö×Ó×é³ÉŗĶ½į¹¹ÉĻĻąĖʵÄÓŠ»śĪļÓŠŅ»“óĄą(Ė×³Ę”°Ķ¬ĻµĪļ”±)£¬ĖüĆĒ¾ł·ūŗĻĶØŹ½ ”£µ±n£½ Ź±£¬ÕāĄąÓŠ»śĪļæŖŹ¼³öĻÖĶ¬·ÖŅģ¹¹Ģ唣
£Ø3£©B¾ßÓŠµÄŠŌÖŹŹĒ (ĢīŠņŗÅ)”£
¢ŁĪŽÉ«ĪŽĪ¶ŅŗĢå ¢ŚÓŠ¶¾ ¢Ū²»ČÜÓŚĖ® ¢ÜĆܶȱČĖ®“ó ¢ŻČĪŗĪĢõ¼žĻĀ²»ÓėĒāĘų·“Ó¦ ¢ŽæÉŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗŗĶäåĖ®¾łĶŹÉ«Š“³öŌŚÅØĮņĖį×÷ÓĆĻĀ£¬BÓėÅØĻõĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø4£©Š“³öÓÉCŃõ»ÆÉś³ÉDµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø5£©CÓėE·“Ó¦ÄÜÉś³ÉĻą¶Ō·Ö×ÓÖŹĮæĪŖ100µÄõ„£¬øĆ·“Ó¦ĄąŠĶĪŖ £»Ęä»Æѧ·½³ĢŹ½ĪŖ£ŗ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«Ź”øßŅ»ĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ijŹµŃ銔×éµÄĶ¬Ń§ÓĆÓŅĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ½ųŠŠµē½ā·“Ó¦£¬µē½ā²ŪČװӊKI-µķ·ŪČÜŅŗ£¬ÖŠ¼äÓĆŅõĄė×Ó½»»»Ä¤øōæŖ”£ŌŚŅ»¶ØµÄµēŃ¹ĻĀĶصē£¬·¢ĻÖ×ó²ąČÜŅŗ±äĄ¶É«£¬Ņ»¶ĪŹ±¼äŗó£¬Ą¶É«Öš½„±äĒ³”£

ŅŃÖŖ:3I2+6OH£= IO3£+5I£+3H2O
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©×ó²ąĪŖµēŌ“__________¼«”£(Ģī”°Õż”±»ņ”°øŗ”±)
£Ø2£©ĒėÓĆ·½³ĢŹ½¼°±ŲŅŖµÄĪÄ×Ö½āŹĶ×ó²ąČÜŅŗ±äĄ¶É«µÄŌŅņ£æ___________________”£
£Ø3£©Š“³öÓŅ²ą·¢ÉśµÄÓŠ¹Ųµē¼«·“Ó¦µÄ·“Ó¦Ź½£ŗ_____________________”£
£Ø4£©µē½ā·“Ó¦½įŹųŹ±£¬×ó²ąČÜŅŗÖŠ»¹_________I£”£(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)
£Ø5£©Š“³öµē½ā²ŪÄŚ·¢Éś·“Ó¦µÄ×Ü»Æѧ·½³ĢŹ½£ŗ_____________________”£
£Ø6£©Čē¹ūÓĆŃōĄė×Ó½»»»Ä¤“śĢęŅõĄė×Ó½»»»Ä¤£¬µē½ā²ŪÄŚ·¢ÉśµÄ×Ü»Æѧ·“Ó¦_________”£(Ģī”°±ä”±»ņ”°²»±ä”±)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓ±±Ź”ø߶žÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ£ŗ4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ”÷H=-1025kJ/mol,øĆ·“Ó¦ŹĒŅ»øöæÉÄę·“Ó¦”£Čō·“Ó¦Īļ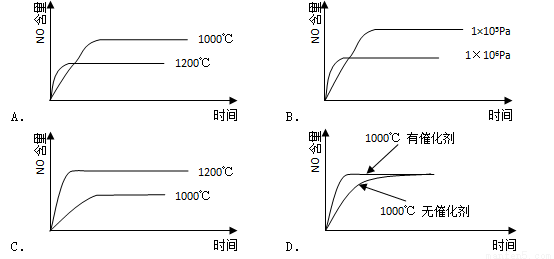
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com